
آنتالپی استاندارد سوختن
چکیده: در ادامه بررسی آنتالپی های استاندارد، به معرفی آنتالپی استاندارد سوختن می پردازیم. با ما همراه باشید.
شرح درس:
به واکنش زیر توجه کنید:

همانطور که می بینید در هنگام سوختن یک مول متان، 890kJ انرژی آزاد می شود. این مقدار برابر با آنتالپی استاندارد سوختن متان است.

• آنتالپی استاندارد سوختن یک ماده، به تغییر آنتالپی فرایندی گفته می شود که طی آن، یک مول از ماده ای در مقدار کافی اکسیژن خالص بسوزد.
متان یک هیدروکربن است. هیدروکربن ها در واقع نوعی سوخت هستند و هرچه مقدار آن ها بر حسب گرم بیش تر باشد مانند این است که مقدار بیش تری سوخت را سوزانده باشیم پس گرمای حاصل نیز بیشتر خواهد بود. بنابراین در مقایسه آنتالپی سوختن هیدروکربن ها در درجه اول به مقدار آن ها بر حسب گرم توجه می کنیم. برای مثال گرمای حاصل از سوختن دو مول متان از گرمای حاصل از سوختن یک مول متان بیشتر است زیرا دو مول متان جرم بیشتری دارد و حاوی سوخت بیشتری است. همچنین آنتالپی استاندارد سوختن بوتان از آنتالپی استاندارد سوختن پروپان منفی تر است. زیرا جرم مولی بوتان بیشتر است و سوخت بیشتری دارد در نتیجه گرمای حاصل از سوختن آن نیز بیشتر است.
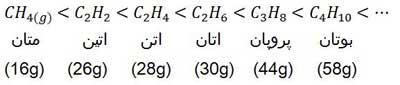
همانطور که ملاحظه می فرمایید جرم مولی اتان بیشتر از اتن و اتن بیشتر از اتین است در نتیجه آنتالپی استاندارد سوختن اتان نیز از اتن بیشتر بوده و آنتالپی استاندارد سوختن اتن از اتین بیشتر است. اما آزمایش نشان داده است که اگر یک دماسنج را در فاصله معینی از شعله این سه هیدروکربن قرار دهیم، شعله اتین از همه داغ تر است و ترتیب دمای شعله به صورت مقابل خواهد بود:
اتان < اتن (اتیلن) < اتین (استیلن)

در حقیقت گرمای حاصل از سوختن با دمای شعله سوختن کاملا متفاوت است. در مقایسه دمای شعله سوختن باید به تعداد مول های گازی حاصل توجه کنیم. 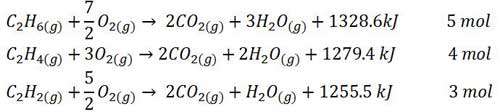
همان طور که مشاهده می شود در سوختن یک مول اتان، 5 مول گاز تولید شده است پس گرمای حاصل از سوختن آن بین 5 مول گاز تقسیم می شود. در سوختن یک مول اتن، 4 مول گاز تولید شده است پس گرمای حاصل از سوختن بین 4 مول گاز تقسیم می شود. هم چنین در سوختن یک اتین 3 مول گاز تولید می شود در نتیجه گرمای حاصل از سوختن آن بین 3 مول گاز تقسیم می شود.
• شعله اتین (استیلن) به قدری داغ است که از آن در جوشکاری استفاده می شود.
از آنجاکه گرمای حاصل از سوختن اتین بین تعداد مول های گازی کمتری تقسیم می شود و میانگین انرژی گرمایی گازهای حاصل از سوختن اتین بیشتر است، دمای شعله آن نیز بالاتر خواهد بود.
حال به واکنش زیر توجه کنید:

معادله واکنش سوختن گرافیت با معادله واکنش تشکیل (CO2(g از عناصر سازنده اش یکسان است بنابراین می توان گفت آنتالپی استاندارد سوختن گرافیت برابر آنتالپی استاندارد تشکیل (CO2(g است. در واقع در برخی از واکنش ها ممکن است ∆H چندین اسم داشته باشد. در این واکنش، ∆H ،هم آنتالپی استاندارد سوختن گرافیت و هم آنتالپی استاندارد تشکیل (CO2(g نام دارد.
مرکز یادگیری سایت تبیان – تهیه و تنظیم: مهسا شاه حسینی

















