ساخت ستون تصفیه آب با نانوفناوری - جلسه اول - آلایندههای آب
جامدات میتوانند به دو صورت معلق و محلول در آب وجود داشته باشند. ذرات جامد معلق در آب ممکن است از ذرات آلی، معدنی و یا امتزاجناپذیر تشکیلشده باشند...

نویسنده : یگانه داودی
بازدید :
زمان تقریبی مطالعه :
تاریخ : سه شنبه 1398/10/17 ساعت 14:32
1-آلایندههای فیزیکی آب
1-1-مواد جامد معلق (TSS)
جامدات میتوانند به دو صورت معلق و محلول در آب وجود داشته باشند. ذرات جامد معلق در آب ممکن است از ذرات آلی، معدنی و یا امتزاجناپذیر تشکیلشده باشند. جامدات معدنی نظیر خاک رس، لای و سایر مواد تشکیلدهنده خاک طبیعی، جامدات آلی نظیر ریشه گیاهان و جامدات بیولوژیکی (سلولهای جلبکی، باکتریها و غیره) را شامل میشوند. مواد جامد معلق که در اثر عملکرد فرسایشی آب جاری بر روی سطح خاک ایجاد میشوند، تحت عنوان آلایندههای طبیعی شهرت دارند. به علت خاصیت جذب خاک، مواد معلق بهندرت در آبهای زیرزمینی یافت میشود.
سایر مواد معلق ممکن است در اثر استفاده انسان از آب به وجود آیند. فاضلاب شهری معمولاً حامل مقادیر قابلتوجهی از جامدات معلق میباشند که ازنظر ماهیت عمدتاً آلی هستند. مصارف صنعتی آب ممکن است منجر به ورود ناخالصیهایی با ماهیت آلی یا معدنی در آب شود. مایعات امتزاجناپذیر نظیر روغنها گریسها که اغلب در فاضلابهای صنعتی دیده میشود. جامدات معلق آلی ممکن است بهصورت بیولوژیکی مورد تجزیه قرار گیرند. جامدات معلق فعال ازنظر بیولوژیکی ممکن است شامل ارگانیزمهای بیماریزا باشند.
1-2- کدورت
کدورت پدیدهای است که میزان شفافیت آب را مشخص میکند و بهعنوان یک خاصیت ظاهری آب محسوب میگردد. کدورت باعث پراکندگی یا جذب نور در حین عبور آن بر روی یک خط مستقیم در آب میشود. اگرچه کدورت به دلیل وجود مواد معلق در آب نیز به وجود میآید، ولی ارتباط دادن با اندازههای کمی مواد معلق در آب مانند شکل، اندازه و ضریب شکست ذرات موجود در سوسپانسیون که همگی در خاصیت پراکنده ساختن نور دخالت دارند، مشکل است، به همین علت کدورت بهعنوان شاخص کمی از ذرات جامد معلق محسوب نمیگردد.
قسمت عمده کدورت در آبهای سطحی از فرسایش مواد کلوئیدی نظیر خاک رس، لای، خردهسنگها و اکسیدهای فلزی خاک حاصل میشود. رشتههای گیاهی و میکرو ارگانیزمها در کدورت آب نقش دارند. فاضلابهای صنعتی و خانگی حاوی مقادیر زیاد مواد کدورت زا میباشند. صابونها، شویندهها و عوامل امولسیون کننده، کلوئیدهای پایداری را تولید میکنند که نهایتاً منجر به کدورت آب میشوند.
1-3- رنگ
آب خالص بیرنگ است، اما آبی که در طبیعت یافت میشود معمولاً به علت وجود مواد خارجی، دارای رنگ میباشد. رنگ آب اگر درنتیجه تأثیر نور بر مواد معلق به وجود آید، اصطلاحاً رنگ آشکار نامیده میشود و رنگی که در اثر مواد جامد محلول پدید آمده است و پس از جداسازی مواد معلق همچنان در آب باقی میماند به نام رنگ حقیقی خوانده میشود. بهعنوانمثال، اکسیدهای آهن، رنگ قرمز کمرنگ به آب میدهند و اکسیدهای منگنز موجب قهوهای و یا تیرهرنگ شدن آب میشوند. پسابهای صنعتی ناشی از صنایع نساجی و عملیات رنگرزی، صنایع غذایی، تولید مواد شیمیایی، استخراج سنگ معدن، پالایش و عملیات مربوط به کشتارگاهها ممکن است در اثر ارتباط با نهرها و رودخانههای طبیعی ایجاد رنگ مینمایند.
1-4- طعم و بو
موادی که در آب ایجاد بو میکنند، عموماً ایجاد طعم نیز مینمایند ولی مواد معدنی زیادی وجود دارند که ایجاد طعم مینمایند اما بههیچوجه بو تولید نمیکنند. مواد معدنی، فلزات، مواد نفتی، محصولات نهایی واکنشهای بیولوژیکی و اجزای تشکیلدهنده فاضلاب در طعم و بوی آب مؤثر هستند. مواد قلیایی طعم تلخی به آب میبخشند درحالیکه نمکهای فلزی عموماً دارای طعم شور یا تلخ میباشند. بخش عمدهای از مواد آلی که در آب ایجاد طعم و بو مینمایند ناشی از تولیدات صنایع نفتی هستند. ترکیبات گوگردی ازجمله مهمترین محصولاتی هستند که در آب، طعم و بوی تخممرغ گندیده را ایجاد مینمایند.
اندازهگیری مواد آلی به وجود آورنده طعم و بو به کمک روشهای کروماتوگرافی گازی یا مایع امکانپذیر است. عامل طعم و بو اغلب برای آبهای آشامیدنی مطرح است. یک حداکثر مقدار (TON) برابر با 3 توسط سازمان بهداشت جهانی توصیهشده است.
1-5- دما
دما برای ارزیابی مستقیم آب آشامیدنی یا فاضلاب بهکاربرده نمیشود ولی یکی از مهمترین مشخصههای آب سطحی در طبیعت به شمار میرود. دمای آب به مقدار زیاد بر گونههای بیولوژیکی موجود در آب و شدت فعالیت آنها مؤثر است. در دماهای بالا، موجودات ذرهبینی که در استفاده از منابع غذایی و تولیدمثل کارایی بیشتری دارند، تکثیر پیدا میکنند درحالیکه سایر موجودات ازلحاظ جمعیتی کاهش مییابند یا بهطورکلی از بین میروند. همچنین غلظت اکسیژن محلول در آب نیز تابعی از دماست و با افزایش دما کاهش مییابد. حداکثر چگالی آب در دمای 4 درجه سانتیگراد است، در هر دو سوی این دما، چگالی آب کاهش مییابد که این خاصیت آب در میان تمام مایعات منحصربهفرد است.
2-آلایندههای شیمیایی آب و فاضلاب
آب بهعنوان حلال عمومی شناختهشده است و کیفیت شیمیایی آب در ارتباط مستقیم با حلالیت آن میباشد. متغیرهای مهم در مسائل مربوط به کنترل کیفیت عبارتاند از:
مقدار کل جامدات محلول (TDS)
مواد محلول از خاصیت آب بر روی جامدات، مایعات و گازها به وجود میآیند. مواد محلول با فیلتر کردن آب تصفیه نمیشود و پس از تبخیر آب بهعنوان جزئی از مواد جامد آب بهصورت رسوب باقی میمانند. مواد محلول نیز ممکن است ازنظر ماهیت، آلی یا معدنی باشند. اندازهگیری مستقیم مقدار کل جامدات محلول، پس از جداسازی مواد جامد معلق، به کمک تبخیر آب امکانپذیر است. وزن رسوب باقیمانده بیانگر مقدار کل جامدات محلول TDS میباشد. مقدار TDS برحسب میلیگرم در لیتر بر مبنای جرم خشک بیان میشود.
هدایت الکتریکی
هدایت الکتریکی (EC) آب معرف قدرت یونی یک محلول برای انتقال جریان است با واحد میکرو زیمنس بر سانتیمتر بیان میشود. در حقیقت واحد هدایت الکتریکی S برابر با عکس مقاومت الکتریکی است،
یعنی: S = Ω−1
رابطهی غلظت کل جامدات با هدایت الکتریکی بهصورت زیر است:
TDS =c (EC)
در این رابطه c یک مقدار ثابت است که از جدول زیر تعیین میشود:
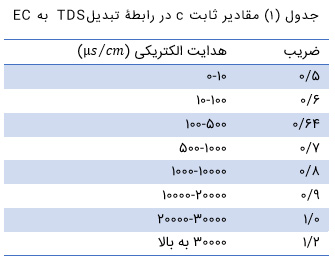
قلیایت به میزان یونهایی از آب که برای خنثیسازی یونهای هیدروژن در واکنش شرکت میکنند اطلاق میشود. قلیایت معیاری برای توانایی آب جهت خنثیسازی اسیدها بهحساب میآید.
اجزای تشکیلدهنده قلیایت در سیستم طبیعی آب عبارتند از:
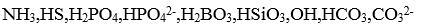
سختی
سختی بهصورت غلظت کاتیونهای چند ظرفیتی در محلول تعریف میشود. سختی بسته به آنیونی که همراه آن است بهعنوان سختی کربناتی و سختی غیر کربناتی طبقهبندی میشود. سختی که ناشی از قلیایت است سختی کربناتی و سختی باقیمانده، سختی غیر کربناتی نامیده میشود. ازآنجاکه غلظت یونهای فلز چند ظرفیتی کلسیم و منیزیم بیش از سایر یونهای چون آهن، منگنز، استرانسیم و آلومینیوم میباشد، برای تمامی مقاصد میتوان سختی را برابر با مجموع یونهای کلسیم و منیزیم در نظر گرفت. سختی را میتوان به کمک تکنیکهای اسپکتروفتومتری و یا تیتراسیون شیمیایی که برای تعیین مقادیر یونهای کلسیم و منیزیم در یک نمونه خاص انجام میگیرد، اندازهگیری کرد.
در ادامه آلاینده های شیمیایی آب را به صورت مختصر معرفی خواهیم نمود.
2-1-فلوراید
فلوراید بهطورکلی در طبیعت در برخی از انواع سنگهای رسوبی یا آذرین یافت میشود. فلوراید بهندرت به مقدار زیاد در آبهای سطحی مشاهده میشود. حداکثر غلطت پیشنهادی برای این متغیر کیفی در آبهای آشامیدنی 5/1 میلیگرم در لیتر میباشد.
2-2-شویندهها
شویندهها ترکیباتیاند که علاوه بر انحلال و پخش در آب قدرت پاککنندگی آن را نیز افزایش دهند. انواع طبیعی پاککنندهها مثل صابون، گل سرشور و غیره از زمانهای قدیم مورداستفاده قرارگرفتهاند آخرین دستگاههای صابون کشفشده، مربوط به 2000 سال پیش است کف کردن صابونها در آبی که املاح کلسیم و پتاسیم داشته باشد به تأخیر میافتد درنتیجه این املاح باعث کاهش قدرت پاککنندگی میشوند. درحالیکه این مشکل به علت فرمول خاص شوینده ها تا حدود زیادی برطرف شده است. شوینده های امروزی غالباً بهصورت سنتتیک (تولیدشده بهصورت مصنوعی) میباشد. ورود این مواد در زندگی انسان بهسرعت باعث کاهش کاربرد انواع طبیعی پاککنندهها شده است.
وجود کف در حوضهای هوادهی در تصفیهخانههای فاضلاب میزان انتقال اکسیژن به فاضلاب را بهشدت تقلیل میدهد بهطوریکه گاهی تقلیل راندمان تصفیه در اثر کف شوینده ها به ۸۰ درصد میرسد. در حوضهای تهنشینی اولیه وجود ماده مؤثر دترجنت مانع تهنشینی کامل مواد معلق میشود و چربی موجود در فاضلاب در اثر کف زیاد به سایر قسمتهای تصفیهخانه نیز راه مییابد ماهیان و آبزیان نیز از آثار سوء شویندهها بیبهره نیستند زیرا شویندهها باعث کاهش میزان اکسیژنگیری آب میشوند. شویندهها قادرند حالت و کیفیت پروتئین را تغییر دهند و متابولیسم باکتریها را مختل سازند و موجب کندی اعمال حیاتی آنها گردند، این امر ناشی از اثر شویندهها در کاهش کشش سطحی آب میباشد غشاء میکرواورگانیزمها در اثر شویندهها پاره شده و موجب از بین رفتن آنزیمها میشود. این موارد در مورد مصرف شویندهایی است که ماده مؤثر آن تجزیه شونده نیست؛ اما مواد مؤثر تجزیه شونده در روشهای تصفیه و دیگر موارد یادشده اشکالات مهمی به وجود نمیآورد.
بهطورکلی آثار سوء حیاتی شویندهها بر محیط زیست عبارتاند از:
تجمع کف بر روی آبهای سطحی و جلوگیری از عمل اکسیژنگیری آب
تولید بو و طعم نامطبوع در آب
اثرات سمی بر موجودات زنده (انسان، موجودات آبی و گیاهان)
تخریب و نابودی اکوسیستمها
حذف و کاهش مواد معلق آب در حضور شویندهها بهصورت دلخواه مقدور نیست
به خودگیری میکروبها بیماریزا و مساعد نمودن شرایط محیطی در جهت شیوع بیماریها
اشکال در امر انعقاد و تهنشینی و صاف کردن آب
وقوع پدیده اوتریفیکاسیون (شکوفایی جلبکی) به لحاظ مصرف فسفاتها
تجزیهناپذیری گروه سخت شوینده ها
ایجاد واکنش فیزیولوژیکی در مصرفکنندگان آب آلوده
سالهای زیادی است که صنایع صابون و دترجنت به دلیل ایجاد آلودگیهایی در آب مانند آلودگی کف و مغذی شدن توجه مسئولان محیط زیست را به خود جلب نموده است. شوینده ها پس از مصرف به همراه پساب به دریاچهها یا رودخانهها ریخته میشوند و بر روی محیطزیست تأثیر مخرب میگذارند.
دترجنت ها قادرند عمل خود پالایی آبها را به تأخیر انداخته و موجب محدودیتهایی در کاهش و حذف مواد آلی شوند. آلکیل سولفاتها نوعی از دترجنت ها (شویندهها) هستند که سریعاً توسط عوامل بیولوژیکی
تجزیه میشوند. بنابراین در آب رودخانه حلشده و مصرف اکسیژن محلول را افزایش میدهند.
غلظتهای زیاد دترجنت ها در حدود ppm۳۰ اثرات سویی بر سیستم تصفیه فاضلاب بیولوژیکی دارد. همچنین دترجنت ها روی میزان هوادهی مجدد آب اثر میگذارند. وجود شوینده ها میزان تهنشینی ذراتی را که اندازه آنها بیش از 25 میکرون باشد افزایش داده ولی میزان تهنشینی ذرات کوچکتر را کاهش میدهد. وجود شوینده¬ها در لجن هضم شده از ارزش کودی آن میکاهد زیرا شوینده های موجود در آن در تماس مستقیم با بذر و ریشه گیاهان قرار میگیرد.
چنانچه شوینده¬ها در حد کمتر از 50 میلیگرم در لیتر آب وجود داشته باشند هیچگونه تغییرات نامطلوبی در مزه آب ایجاد نمیکنند. احتمالاً تغییراتی که شویندهها در مزه آب ایجاد میکنند مربوط به خود شوینده¬ها نبوده بلکه صرفاً به مواد سازنده یا عطر آنها مربوط میشود.
2-3- فلزات غیر سمی
همه فلزات تااندازهای در آب قابلحل میباشند. پیدایش فلزات در آبهای طبیعی از طریق حل شدن آنها در آب، توسط رسوبات و تخلیه فاضلابهای شهری، صنعتی و کشاورزی صورت میگیرد. مقدار فلزات داخل آب معمولاً توسط روش جذب اتمی اندازهگیری میشود.
علاوه بر یونهای کلسیم و منیزیم که باعث سختی در آب میشوند، سایر فلزات غیر سمی مانند آهن، منگنز، آلومینیوم، مس و روی نیز در آب وجود دارند. آهن و منگنز که در بسیاری از موارد به همراه یکدیگر مشاهده میشوند در غلظتهای معمولی علائمی دال بر خطرناک بودن برای سلامتی انسان بروز نمیدهند. غلظت آهن بیش از mg/L 3/0 و غلظت منگنز بیش از mg/L 05/0 میتواند رنگ آب را تغییر دهد.
2-4-فلزات سمی
فلزاتی که وجودشان حتی به مقدار کم برای سلامت انسان مضر است، سمی تلقی میشوند. فلزات سمی در آب شامل آرسنیک، باریم، کادمیم، کروم، سرب، جیوه و نقره میباشند. غلظتهای زیاد فلزات سنگین مانند آرسنیک، کادمیم، سرب و جیوه برای سلامتی انسان خطرآفرینی خاصی دارند. فلزات مذکور توسط زنجیره غذایی موجود در طبیعت تغلیظ میشوند و بدین ترتیب بزرگترین خطر را برای ارگانیزمهای نزدیک به قسمت بالایی زنجیره ایجاد میکنند. غلظتهای قابلملاحظهاین فلزات غالباً در پسابهای معدنی، صنعتی و زه آبهای کشاورزی وجود دارند.
2-5-مواد آلی
بسیاری از مواد آلی در آب محلول هستند. اغلب ترکیبات آلی طبیعی از تجزیه مواد آلی جامد تشکیل میشوند، درحالیکه آن دسته از مواد آلی که از طریق مصنوعی تهیه میشوند، معمولاً درنتیجه تخلیه فاضلابهای شهری، صنعتی و زه آبهای کشاورزی به محیط زیست وارد میشوند.
مواد آلی حلشده در آب معمولاً به دو گروه اصلی مواد آلی قابلتجزیه توسط فعالیتهای بیولوژیکی و غیرقابل تجزیه توسط فعالیتهای بیولوژیکی تقسیم میشوند.
مواد قابلتجزیه آن دسته از مواد هستند که میتوانند بهراحتی بهعنوان مواد غذایی توسط میکرو ارگانیزمهای طبیعی مورداستفاده قرار بگیرند. این مواد محلول معمولاً شامل نشاسته، چربیها، پروتئینها، الکلها، اسیدها، آلدئیدها و استرها میشوند. مصرف مواد آلی محلول توسط میکرو ارگانیزمها ممکن است همراه با فرایندهای اکسیداسیون و احیا باشد. فرایند اکسیداسیون، در صورت وجود اکسیژن، نسبت به فرایند احیاء مؤثرتر است.
در محیطهایی که اکسیژن حضور دارد، فرآیندها هوازی است و محصولات نهایی مواد آلی پایدارند و برای محیط زیست ضرر ندارند. در صورت عدم حضور اکسیژن منجر به ایجاد محصولاتی ناپایدار خواهد شد. میزان مواد آلی عمدتاً توسط متغیرهای کیفی BOD وCOD بررسی میشود.
2-6-اکسیژن موردنیاز بیولوژیکی (BOD)
بر اساس این شاخص، آن قسمت از آلایندههای آلی که باکتریها قادر به تجزیه آنها هستند، تعیین میشود.
تجزیه مواد آلی توسط باکتریها (بهطور طبیعی) به دما و زمان بستگی دارد، مقدار این متغیر کیفی در دمای 20 درجه سانتیگراد اندازهگیری میشود. تجربه نشان داده که BOD یک نمونه در ساعات و حتی روزهای اولیه متفاوت میباشد. امروزه در سطح جهانی مقدار این شاخص در طی پنج روز را بهعنوان استاندارد انتخاب کرده، آن را بهصورت BOD5 نشان میدهند.
BOD5 کاهش اکسیژن در نمونه را (که طی پنج روز توسط باکتریهای هوازی مصرف میشود تا مواد آلی را تجزیه کنند)، با غلظت مواد آلی قابلتجزیه توسط باکتریها مرتبط میسازد. بالا بودن BOD معرف شدت فسادپذیری نمونه است.
2-7-مواد آلی غیر قابلتجزیه توسط فعالیتهای بیولوژیکی
برخی از مواد آلی در برابر تجزیه بیولوژیکی از خود مقاومت نشان میدهند. سلولز و فنل ها که در سیستمهای طبیعی یافت میشوند بهقدری آهسته تجزیه میشوند که معمولاً آنها را غیرقابلتجزیه معرفی میکنند.
مولکولهایی که دارای پیوندهای فوقالعاده قوی هستند (نظیر برخی از پلی ساکاریدها) و مولکولهای با ساختمانهای حلقوی (نظیر بنزن، ترکیبات آلی که در نفت خام و یا در فرآیند پالایش نفت) اساساً غیر قابلتجزیهاند.
2-8- اکسیژن موردنیاز شیمیایی (COD)
منظور از این شاخص تعیین مقدار کل مواد آلی موجود در آب است. این شاخص هم معرف مواد آلی قابلتجزیه و هم غیر قابلتجزیه توسط باکتریها میباشد. آزمایش COD در زمان کمی (تقریباً 3 ساعت) قابل انجام میباشد بنابراین با توجه به همبستگی بین غلظت BOD و COD عموماً بجای آزمایش BOD که چند روز به طول میانجامد، آزمایش COD جهت تخمین BOD نهایی مورداستفاده قرار میگیرد.
اندازهگیری کل مواد آلی آب معمولاً به کمک آزمایش اکسیژن موردنیاز شیمیایی (COD) یا آزمایش کل کربن آلی به دیاکسید کربن (TOC) انجام میشود. برای به دست آوردن مقدار مواد آلی غیر قابلتجزیه باید BOD را از COD یا TOC کم کرد. کمیت و کیفیت ترکیبات خاص آلی به کمک روشهای چون گاز کروماتوگرافی قابلاندازهگیری است.
2-9- مواد مغذی
مواد مغذی عناصری هستند که برای رشد و تولیدمثل گیاهان و جانوران ضروریاند. گروه وسیعی از مواد معدنی و عناصر نادر را میتوان بهعنوان مواد مغذی طبقهبندی نمود، لیکن خانواده کربن، نیتروژن و فسفر مهمترین موادی هستند که به مقدار قابلملاحظهای توسط گونههای آبزی مصرف میشود.
2-10- کربن
سلولهای موجودات زنده از کربن، هیدروژن، اکسیژن، ازت و برخی مواد دیگر تشکیلشده است. کربن در رابطه با تشکیل و فعالیت زیستی سلولها، از اهمیت بالایی برخوردار است ولی همواره به مقدار موردنیاز موجود نمیباشد. بخش عمده مواد آلی موجود در چرخه کربن، حاصل فرآیند فتوسنتز است. در این فرآیند دیاکسید کربن مصرفشده، اکسیژن تولید میشود و یک گرم اکسیژن آزاده شده متناظر با 93/0 گرم هیدراتکربن است. سلول گیاهی، گلوکز را به ترکیبات متعددی تبدیل میکند و جانوران، مواد آلی را بهطور مستقیم (گیاه خوران) غیرمستقیم (گوشت خوران) مصرف میکنند.
2-11-نیتروژن
نیتروژن در محیط آبی عمدتاً از منابعی غیر از نیتروژن در اتمسفر تأمین میشود. نیتروژن جزئی از پروتئینهاست و همچنین در کلروفیل و در بسیاری از ترکیبات بیولوژیکی دیگر یافت میشود. منابع نیتروژن در سیستمهای آبی میتوان به فضولات جانوران، مواد شیمیایی و فاضلابهای تخلیهشده اشاره نمود. ترکیبات نیتروژن میتواند اکسیدشده، توسط باکتریهای موجود در خاک تبدیل به نیترات شوند و به سفرههای آب زیرزمینی نفوذ نمایند. بهطورکلی نیتروژن به دو صورت نیتروژن آلی و نیتروژن معدنی شامل آمونیاک، نیترات و نیتریت وجود دارد. به همین دلیل و نیز چون نیتروژن آلی قابلتبدیل به آمونیاک است، اغلب در فاضلابها و آبهای آلوده به فضولات انسانی و حیوانی، آمونیاک، نیتروژن آلی و نیتروژن کجلدال و در نمونههای آب تمیز و فاضلاب تصفیهشده، نیترات و نیتریت مورد آزمایش قرار میگیرد.
2-12- آمونیاک
یونهای نیترات و آمونیاک ازجمله مهمترین آلایندههای آبهای سطحی و زیرزمینی میباشند که علاوه بر چرخه طبیعی ازت در اثر ورود فاضلاب خام انسانی و صنعتی فاضلابهای کشاورزی مواد زائد شهری و صنعتی، تخریب جنگلها و مراتع نیز وارد منابع آب شده و میتوانند اثرات نامطلوبی بر سلامتی مصرفکنندگان برجای بگذارند. مقدار آمونیاک آب نشانگری عالی از آلودگی آب به فاضلاب است. مواد پروتئینی موجود در مدفوع، تجزیه و تبدیل به ازت میشود که خود براثر اعمال میکروبها تبدیل به آمونیاک میشود. آمونیاک آزاد و املاح آمونیاک در آب آشامیدنی نباید از پنجاه میلیگرم در لیتر باشد.
2-13-نیترات
نیترات (NO3-) یکی از آنیونهای معدنی است که درنتیجه اکسیداسیون نیتروژن عنصری حاصل میشود. این ماده یکی از عناصر بسیار ضروری برای سنتز پروتئین در گیاهان است و نقش مهمی در چرخه نیتروژن دارد، نیترات از طریق اکسیداسیون طبیعی تولید و بنابراین در تمام محیط زیست یافت میشود.
فاضلابهای شهری، صنعتی، مواد دفعی حیوانی و گیاهی در شهرهای بزرگ که دارای نیتروژن آلی هستند به خاک دفع میشوند. در اثر فعالیت میکرو ارگانیزمهای خاک نیتروژن آلی به یون آمونیوم (NH4+) تبدیلشده که به این پدیده آمونیفیکاسیون گفته میشود. خاک توانائی نگهداری این ترکیب را در خود دارد اما بهمرور طی پدیده دیگری به نام نیتریفیکاسیون بخشی از یون آمونیوم ابتدا به نیتریت (NO2-) و سپس به نیترات تبدیل میشود لایه سطحی خاک قادر به حفظ و نگهداری این دو ترکیب نبوده و درنتیجه نیتریت و نیترات به آبهای زیرزمینی راه مییابند.
تحقیقات نشان میدهد در مناطقی که دفع فاضلاب بهصورت سنتی و از طریق چاههای فاضلاب انجام میشود، به دلیل نفوذ فاضلاب به سفرههای آب زیرزمینی، میزان نیترات موجود در آب بسیار بالاست. همچنین در شهرهای صنعتی به دلیل وارد شدن آلایندههای صنعتی و زه آب کشاورزی به سفرههای آب زیرزمینی، میزان نیترات آب بسیار بالاست.
نیتریتِ حاصل از احیای نیترات معدنی و آلی، پس از ورود به سیستم گردش خونآهن هموگلوبین را اکسید نموده و از ظرفیت II به ظرفیت III تبدیل مینماید که درنتیجه هموگلوبین به متهموگلوبین تبدیلشده که ظرفیت اکسیژنرسانی بسیار کمتری از هموگلوبین دارد و درنتیجه به بافتها اکسیژن کافی نمیرسد بعد از مدتی رنگ پوست (در ناحیه دور چشم و دهان) به تیرگی میگراید و ازاینرو به آن سندرم BIueBaby میگویند.
این عارضه اولین نشانه مسمومیت با نیترات است و نوزادان زیر شش ماه آسیبپذیرترین گروه سنی در این مورد هستند؛ زیرا نوزادان برخلاف بزرگسالان علاوه بر pH بالای معده و زیادی باکتریهای طبیعی احیاء کننده نیترات فاقد آنزیم برگشت دهنده متهموگلوبین به هموگلوبین هستند. از دیگر علائم افزایش متهموگلوبین میتوان به سردرد خوابآلودگی و اشکال در تنفس اشاره نمود.
احتمال اینکه نیترات معدنی و یا آلی بهعنوان یک عامل سرطانزا عمل نمایند بستگی به احیای نیترات به نیتریت و واکنشهای بعدی نیتریت با سایر مولکولها بهخصوص آمینهای نوع دوم، آمیدها وکارباماتها دارد که منجر به تشکیل ترکیبات nitroso-N میگردد. مطالعات انجامشده در کلمبیا نشان داده که رابطه معنیداری بین شیوع سرطان معده و غلظت نیترات در آب آشامیدنی برداشتشده از چاهها وجود دارد.
با توجه به مطالعات بهعملآمده توسط سازمان بهداشت جهانی در مورد نیترات، این سازمان حداکثر مجاز 50 میلیگرم در لیتر (برحسب نیترات) را اعلام نموده است. استاندارد ملی ایران نیز برای نیترات همین مقدار میباشد. سازمان حفاظت محیط زیست ایالاتمتحده حداکثر مجاز نیترات را 10 میلیگرم بر لیتر (برحسب نیتروژن) قرار داده که معادل با 82/44 میلیگرم در لیتر برحسب نیترات است.
امروزه با رشد روزافزون جمعیت در شهرهای بزرگ آلودگی آب آشامیدنی رو به افزایش است. دفع نادرست فاضلابهای شهری از طریق چاههای جذبی، مصرف بیرویه مواد شوینده و پاککننده بهداشتی که از طریق چاههای جذبی فاضلاب به اعماق زمین نفوذ کرده و سفرههای آب زیرزمینی را آلوده میکنند، استفاده از کودهای شیمیایی و حیوانی، استفاده از آفتکشها و حشرهکشها و... ازجمله دلایل اصلی آلودگی آب آشامیدنی انسانها هستند. وجود این ماده خطرناک در آب آشامیدنی خصوصاً برای نوزادان و زنان باردار عوارض جبرانناپذیری را در پی خواهد داشت.
2-14- نیتریت
مقدار نیتریتهای آب آشامیدنی باید صفر باشد و بودن آنها نشانه آلودگی تازه است، اما در آب چاههای عمیق ممکن است نیتریتها یافت شوند؛ بنابراین آبهای دارای نیتریت باشد مشکوک به شمار میآیند مگر آنکه از چاه عمیق بهدستآمده باشند. نیتریت نشانه پیشینه آب است و بودن آنها در آب، نشانه آلودگی پیشین است.
2-15- فسفر
فسفر موجود در فاضلاب به سه صورت ارتوفسفات، پلی فسفات و فسفر آلی وجود دارد. 70% فسفر در فاضلاب خام شهری بهصورت پلی فسفات و فسفات آلی وجود دارد و 10% آن بهصورت معلق میباشد که در مخزن تهنشینی اولیه حذف میشود و 10 تا 30 درصد فسفر ورودی نیز در سنتز سلولی میکروارگانیسمها مصرف میشود.
فسفات اثرات زیادی بر موجودات زنده دارد. اثر فسفات نتیجه انتشار وسیع آن در محیط زیست به دلیل معدنکاری و کشت و زرع میباشد. در هنگام تصفیه آب معمولاً فسفات از بین نمیرود، بنابراین فسفات میتواند در مسافت زیادی از طریق آبهای سطحی انتشار پیدا کند. با توجه به مقدار اضافه فسفر در طبیعت که به دلیل فعالیتهای انسانی اتفاق افتاده است و به دلیل افزایش غلظت فسفر، در چرخه فسفر اختلالاتی پدید آمده است.
با افزایش غلظت فسفر در آبهای سطحی، تعداد ارگانیسمهای وابسته به فسفات افزایش مییابد. این ارگانیسمها که عبارتاند از جلبک و خزه، مقدار زیادی از اکسیژن محیط را مصرف میکنند و از وارد شدن نور خورشید به آب جلوگیری میکنند. این مسئله باعث میشود که سایر موجودات زنده نتوانند در آب زندگی کنند. به این پدیده یوتریفیکاسیون گفته میشود.
تخلیه آبهای حاوی فسفر در منابع آب پذیرنده باعث رشد بحرانی جلبکها میگردد و به دلیل غلظت فسفر موجود در فاضلابهای شهری، میتوان از آنها بهعنوان محلولی تأثیرگذار در این رابطه نام برد. پلی فسفاتها در مواد شوینده، مصرف مواد غذایی پروتئینی و تخلیه مقدار قابلتوجهی فسفر به همراه ادرار در فاضلابهای خانگی در این امر مؤثر هستند.
هر فرد در روز حدود 5/1 گرم تا 5/3 گرم فسفات دفع میکند که این امر بر میزان غلظت فسفاتها در منابع آب میافزاید.
فسفر بهکندی از مواد تهنشین شده در زمین و رسوبات به زندگی ارگانیزمها حرکت میکند و همچنین بسیار کندتر به خاک و رسوبات آبی برمیگردد. گیاهان فسفاتها را از خاک جذب کرده و آنها را در زنجیره غذایی قرار میدهند. بعد از مرگ، گیاهان و یا حیوانات تجزیهشده و مجدداً فسفاتها به خاک برمیگردند. رواناب ممکن است آنها را به اقیانوس منتقل کرده و یا اینکه در اثر تهنشینی و رسوب مجدداً به سنگهای فسفاته تبدیل شوند.
تأثیر انسان در چرخه فسفر عمدتاً از طریق تولید و استفاده از کودهای سنتز تجاری است. فسفات از طریق معدنکاری مواد تهنشین شده عمده از فسفات کلسیم با نام آپاتایت است. گیاهان ممکن است قادر به استفاده از همه کود فسفاته به کار رفته نباشند لذا قسمت اعظم آن بهواسطه جریان سطحی آب منتقل میشود. فسفات موجود در آب سرانجام بهعنوان رسوبات در اعماق آب تهنشین میگردد. در برخی دریاچهها و استخرها ممکن است مجدداً بهصورت ماده مغذی در چرخه قرار گیرد.
همچنین وجود مقادیر زیاد فسفات در آب شرب موجب بیماریهایی ازجمله بیماریهای کلیوی و پوکی استخوان در انسان میشود.
3-آلایندههای میکروبی فاضلاب
3-1-اشرشیا کلی
اشریشیا کُلی (نام علمی: Escherichia coli) یا بطور اختصار E.coli، نوعی باسیل گرم منفی از خانواده انتروباکتریاسهاست که بطور شایع در روده جانوران خونگرم وجود دارد. بیشتر سویههای اشریشیا کلای بیآزار هستند اما برخی از سروتیپها موجب مسمویت غذایی و اسهال میشوند. این باکتری شایعترین عامل عفونت دستگاه ادراری است که حدود ۹۰ درصد عفونتهای ادراری در زنان جوان را به خود اختصاص میدهد. علائم بالینی این عفونت به صورت تکرر ادرار، سوزش ادراری، خون و چرک در ادرار است. با توجه به سرعت تولید مثل بسیار بالای این گونه و مقاومت زیاد، لازم است که کلیه سلولهای این گونه باکتریایی از جریان فاضلاب طی فرآیند تصفیه حذف شود. زیرا باقیماندن آن در پساب موجب آلوده شدن منابع پذیرنده و گسترش سریع آلودگی خواهدشد.
انتروکوک
انتروکوکها، کوکسیهای گرم مثبت بوده که به صورت جفت (دیپلوکوک) یا زنجیرههای کوتاه دیده میشوند. تمایز انتروکوکها از استرپتوکوکها از روی ویژگیهای ظاهری، بسیار مشکل است. دو گونه مهم همزیست از انتروکوک در روده انسان (مدفوع) عبارتند از: انتروکوک فکالیس (۹۰% تا ۹۵%) و انتروکوک فاسیوم (۵% تا ۱۰%). بدنه اصلی شاخص کلیفرم مدفوعی که در تستهای آب و فاضلاب رایج است را باکتری انتروکوک تشکیل میدهد. مهمترین عفونتهای ایجاد شده توسط انتروکوکها عبارتند از: عفونتهای مجرای ادراری، باکتریمی، اندوکاردیت و مننژیت. برخی از انتروکوکها بطور ذاتی به آنتی بیوتیکهای بتالاکتام (پنی سیلین، سفالوسپورینها و کارباپنم) و آمینوگلوکوزیدها مقاوم هستند. در دو دهه گذشته، سویههای انتروکوکی مقاوم به وانکومایسین (VRE) در بیماران بستری در بیمارستانها افزایش یافتهاند. این باکتریها نسبت به تغییرات pH بسیار مقاوم بوده و ماندگاری بالایی در منابع آب، بهویژه آبهای زیرزمینی خواهند داشت.
3-3-تخم انگل نماتود
نماتدها به گروهی از جانوران پرسلولی و کرمی یا نخی شکل گفته میشود که دارای ساختمان غیر بندبند هستند و در یک یا دو انتها ممکن است باریکتر شده باشند. نماتدها از بیمهرگان هستند و در یک انتهای بدن سر و در انتهای دیگر دُم قرار دارد. نماتدها رشته ای یا کرمی شکل بوده ولی ماده برخی از آنها ممکن است متورم و باد کرده باشد. حدود 1500 گونه نماتد شناخته شده است که فقط 10% آنها انگل گیاهان میباشند. تقریباً در هر یک گرم خاک مرطوب100-5 نماتد وجود دارد که از نظر تنوع بسیار متغیر میباشد و بسیاری از آنها از باکتری ها، قارچ ها، جلبک ها و سایر نماتد ها تغذیه میکنند. نماتدها آفت بسیار خطرناکی برای گیاهان بوده و میتوانند در صورت انتشار در محیط، بهخصوص در زمینهای کشاورزی، اکوسیستم گیاهی را دستخوش تغییر نمایند.
برای مطالعه بیشتر میتوانید به مقالات موجود در سایت باشگاه نانو به آدرس www.nanoclub.ir مراجعه نمایید. نمایید.
مطالب مرتبط:
شما عزیزان می توانید برای انجام این پروژه به طرح درس های ذیل مراجعه فرمایید:
1- آلایندههای آب
2- روشهای تصفیه آب
3- آشنایی با نانوزئولیت
4- سختیگیری و حذف کاتیون از آب زیرزمینی با استفاده از زئولیتهای طبیعی
5- طراحی ستون نمکزدایی از آب
بخش پژوهش های دانش آموزی تبیان

















