ساختار مولکول ها (1)
پیوندهای شیمیایی را بر اساس این که الکترون ها تا چه اندازه ای به هر یک از اتم های پیوند تعلق دارند به دو دسته یونی و کووالانسی تقسیم می کنند.
همان طور که می دانید، پیوندهای شیمیایی اتم ها در یک مولکول کنار یکدیگر نگه می دارد. مثلا هر مولکول H2 هر اتم هیدروژن الکترون 1s خود را برای تشکیل پیوند به اشتراک می گذارد و این الکترون به طور مساوی به دو اتم هیدروژن تعلق دارد، که این پیوند یک پیوند کووالانسی می باشد.
نظریه پیوند ظرفیت (V .B .T): این نظریه به منظور بسط و تعمیم نظریه هایتلر- لاندن و نیز توجیه خصلت جهت دار بودن پیوندهای کوالانسی، توسط پائولینگ و اسلیتر در سال 1931 ارائه شد و بر پایه دو فرض اساسی، یعنی، حالت والانس (حالت برانگیخته) اتم و هیبریداسیون اوربیتال های لایه ظرفیت اتم مرکزی استوار است و اهمیت آن در پیشگویی شکل هندسی مولکول ها و یون ها است. براساس این نظریه، ترکیبات پایدار، از پرشدن تمام اوربیتال های پیوندی یا غیرپیوندی لایه ظرفیت اتم ها حاصل میشوند و یک ترکیب موقعی بالاترین پایداری خود را بدست میآورد که اتم مرکزی آن به بالاترین عدد کوئوردیناسیون (بالاترین تعداد پیوند کوالانسی) خود برسد.
شکل مولکول یا یون عمدتاً با توجه به خصلت جهتدار بودن اوربیتال های اتمی قابل پیشگویی است. هر پیوند کوالانسی را بر اثر همپوشانی دو اوربیتال اتمی و تشکیل اوربیتال مولکولی پیوندی که دو الکترون پیوندی براساس اصل طرد پائولی با اسپین های ناهمسو در آن قرار میگیرند (تا دافعه بین آنها به حداقل برسد)، بین دو اتم برقرار میشود. اوربیتال های مولکولی، از نظر عدد کوآنتومی، مفهوم فیزیکی تابع موج، احتمال و غیره، تفاوت اساسی با اوربیتال های اتمی تشکیلدهنده خود ندارند و انرژی آنها برابر مجموع انرژی الکترون های پیوندی است. مهمترین تفاوت اوربیتال های اتمی و مولکولی در این است که گسترش طولی اوربیتال های مولکولی بیشتر است و الکترون ها در آن تحت جاذبه هر دو هسته قرار دارد.
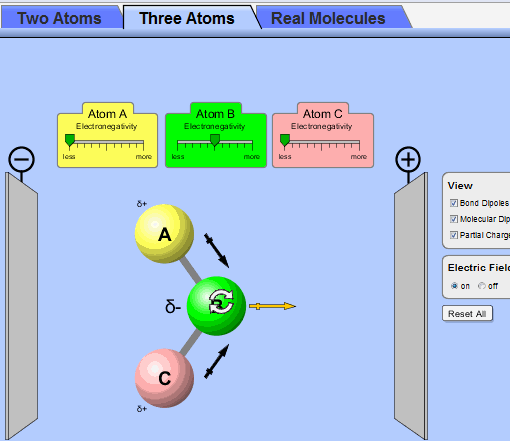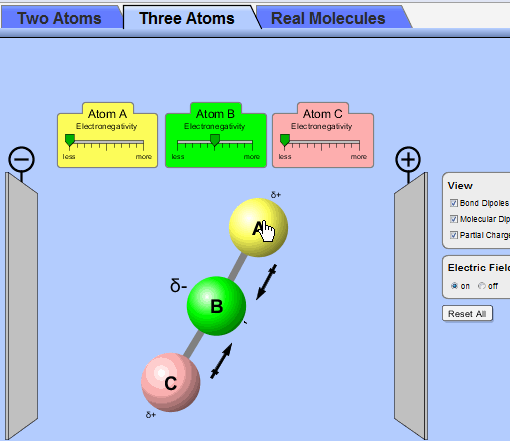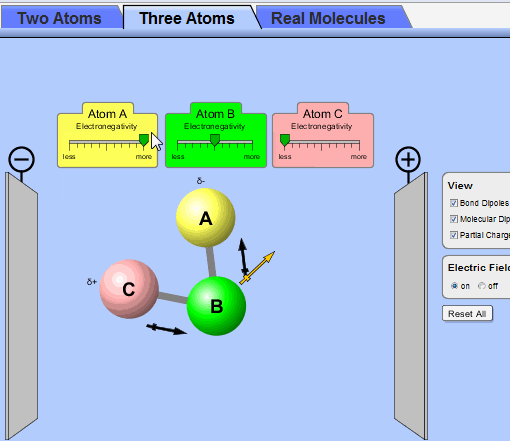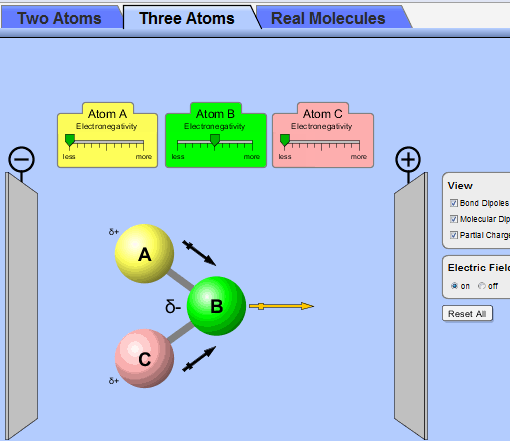
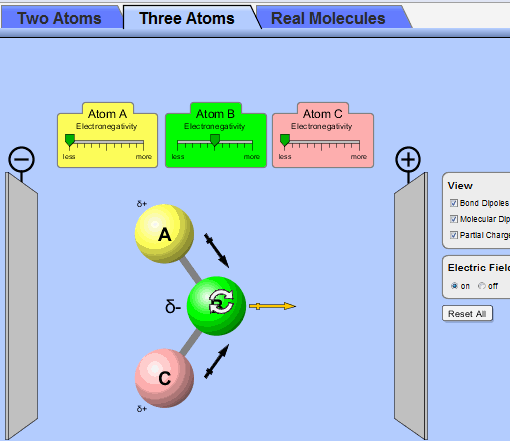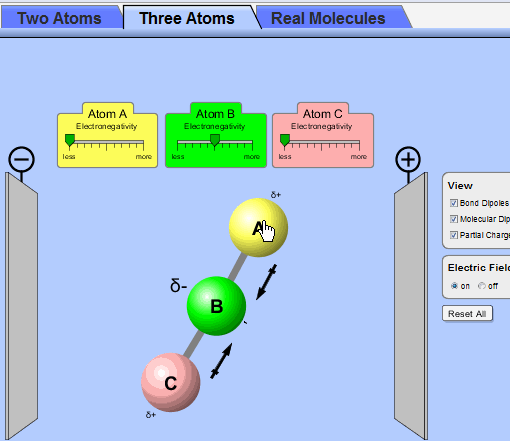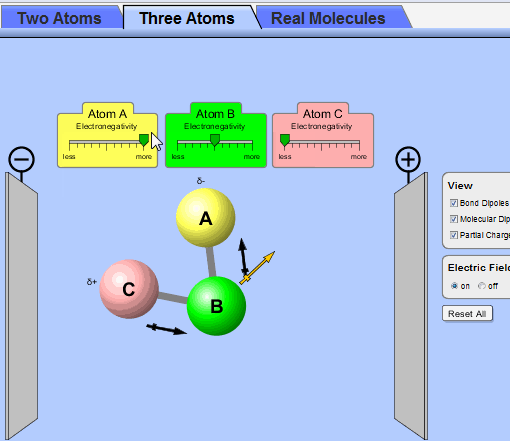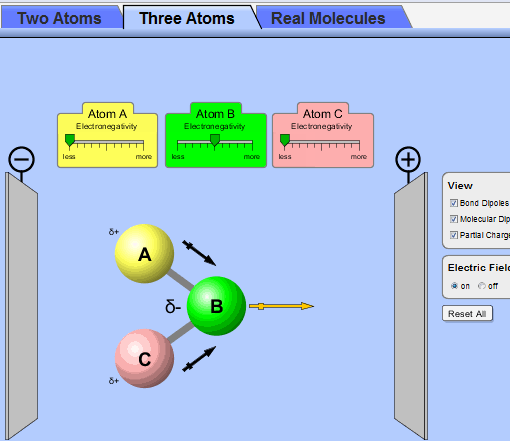
نوع پیوند را با استفاده از خاصیت بنیادی به نام الکترونگاتیوی پیش بینی می کنند. تشکیل پیوند را معمولا می توانیم با در نظر گرفتن این که یک پیوند شیمیایی بازتابی از پایداری پیکر بندی الکترونی ns2np6 گازهای نجیب باشد، درک نمود. اگر یک اتم با از دست دادن، گرفتن یا به اشتراک گذاشتن الکترون بتواند پیوند تشکیل دهد و به این پیکر بندی الکترونی برسد، پایدار خواهد شد، که این قاعده را قاعده هشتایی می نامند و در مورد عنصرهای سبک تر و گروه های IA، IIA، VA، VIA و VIIA جدول تناوبی به استثنای هیدروژن و هلیم که می توانند تنها دو الکترون والانس بپذیرند، صدق می کند. (با وجود این که تشکیل تعداد زیادی از پیوندها از قاعده هشتایی پیروی نمی کند، اما این قاعده غالبا نقطه شروع خوبی برای تعبیر پیوند در مول ها می باشد.)
در مطالب قبل با تعریف پیوند کووالانسی که یک جفت الکترون مشترک بین دو هسته یک پیوند کووالانسی تشکیل میدهند آشنا شده اید.
حال متداول ترین علامت گذاری که شیمی دان ها برای نشان دادن پیوند در مولکول های کووالانسی از آن استفاده می کنند را که تصویر الکترون نقطه ای می باشد مورد بررسی قرار می دهیم. (این مدل اولین بار توسط جی. ان. لوویس ابداع شده است.)
علامت گذاری بر پایه قواعد زیر استوار می باشد:
1- تنها الکترون های والانس نشان داده می شوند.
2- جفت الکترون پیوندی با یک خط تیره بین دو اتمی که الکترون ها را به اشتراک می گذارند نشان داده می شود. بنابر این هنگامی که دو اتم یک جفت الکترون به اشتراک می گذارند با یک خط تیره که پیوند یگانه نام دارد، هنگامی که دو جفت الکترون به اشتراک می گذاردند با دو خط تیره که پیوند دوگانه ناک دارد و هنگامی که سه جفت الکترون به اشتراک می گذارند با سه خط تیره که پیوند سه گانه نام دارد، به یکدیگر متصل می شوند.
3- جفت الکترون غیر مشترک یا غیر پیوندی با یک جفت نقطه در کنار اتمی که به آن تعلق دارد، نوشته می شود.
4- همه الکترون های والانس هر اتم با نقطه یا خط تیره نشان داده می شوند.
برخی خواص الکترونی عناصر که در نوشتن ساختار لوویس به ما کمک می کنند عبارتند از:
1- هیدروز نمی تواند بیش از دو الکترون بپذیرد.
2- کربن، نیتروژن، اکسیژن و فلوئور در ترکیبات پایدار هرگز با بیش از هشت الکترون احاطه نمی شوند (قاعده هشتایی) و تنها در مواردی معدود نیتروژن با تعداد الکترون کمتر احاطه می شود.
3-ترکیبات بیشتر عناصر دیگر در اطراف همه اتم ها غالبا هشتایی دارند. البته استثناهای زیادی در میان عناصر سنگین تر بعد از سیلسیم وجود دارد.
4-عناصر گروه IIIA غالبا هشتایی های ناقص دارند.
5-ترکیباتی که تعداد الکترون های والانس آنها فرد است، حداقل یک اتم دارند که از قاعده هشتایی پیروی نمی کند.
در بسیاری از موارد شما می توانید با پیروی از سلسله مراحل زیر به ساختار لوویس صحیح یک ترکیب برسید. این روش را برای نیتریک اسید، HNO3 شرح می دهیم.
مرحله اول: تعداد کل الکترون های والانس را با جمع کردن تعداد الکترون های والانس هر یک از اتم های مولکول تعیین کنید. تعداد الکترون های والانس یک اتم در گروه A جدول تناوبی برابر با شماره آن گروه می باشد. بنابراین، عناصر گروه IA یک الکترون والانس و عناصر گروه IIA دو الکترون والانس دارند و به همین ترتیبف الکترون های والانس عناصر گروه VIIA برابر با هفت می باشد. چنین ارتباط ساده را نمی توان برای عناصر گروه های B جدول تناوبی به کار برد. تعداد الکترون های والانس در HNO3 برابر است با 24=1+5+(6×3)
مرحله دوم: حال با قرار دادن یک خط تیره (یک جفت الکترون) بین دو اتم، همه اتم های مولکول را به یکدیگر متصل کنید. ممکن است که برای اتصال صحیح اتم ها به اطلاعات خاصی نیاز داشته باشید.
الف) هیدروژن می تواند تنها یک جفت الکترون و بنابراین، تنها یک پیوند داشته باشد.
ب) پیوند اکسیزن-اکسیژن را نمی توان به طور طبیعی یافت. به استثنای پروکسیدها که در آنها دو اتم اکسیژن با یکدیگر پیوند برقرار کرده اند.
ج) گاهی اوقات مشاهده تجربی لازم می باشد. مثلا در N2O، اتصال پیوندها به صورت N-N-O است و نه N-O-N.
د) در همه اکسی اسیدهای معدنی حداقل یک H به اکسیژن متصل می باشد.
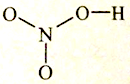
بنابراین در مورد HNO3 می نویسیم:
زیرا می دانیم نیتریک اسید، اکسی اسیدی معدنی است.
توجه: قاعده هشتایی اتصال بیش از چهار اتم به یک اتم مرکزی را منع می کند. اتصال اتم ها دشوارترین بخش نوشتن ساختارها می باشد. اما با درک حقایق بیشتر، این قسمت آسان خواهد شد.
ادامه دارد ...
ساختار مولکول ها (2)
منبع:
http://chimi12.blogsky.com
مرکز یادگیری سایت تبیان - مرجان سلیمانیان