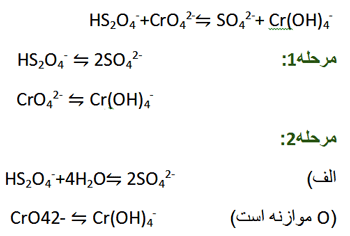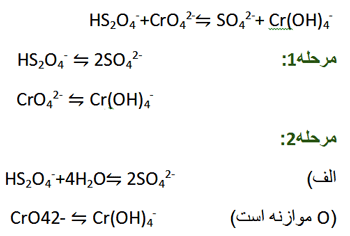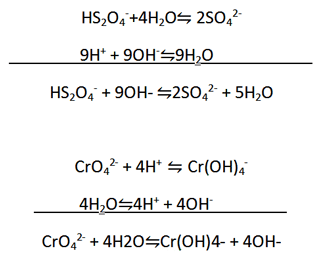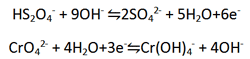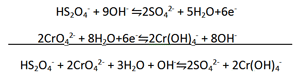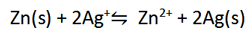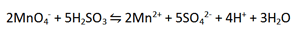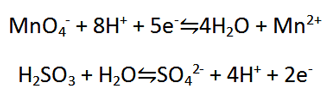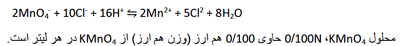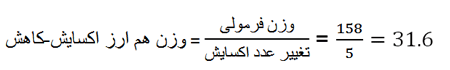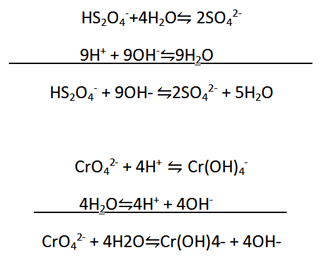حل مسائل اکسایش-کاهش 2
اکسایش نتیجه از دست دادن الکترون و کاهش نتیجه به دست آوردن الکترون است.
در مطلب قبل دانستید که در هر معادله اکسایش-کاهش موازنه شده، تعداد کل الکترون های از دست رفته توسط عنصر یا عنصرهایی که اکسید شده اند باید با تعداد کل الکترون های گرفته شده توسط عنصر یا عنصرهایی که کاهش یافته اند برابر باشد.
واکنش اکسایش – کاهش:
فرایندی که در آن عدد اکسایش عنصرها تغییر کند، فرایند اکسایش – کاهش نامیده می شود.
حال برای آشنایی و درک بهتر موازنه کردن فرایندهای اکسایش-کاهش، این بار محلول بازی را مورد بررسی قرار می دهیم.
در تیتراسیون های اکسایش –کاهش نیز اکثر شناساگرهای مورد استفاده در تیتراسیون های اکسایش-کاهش خود عوامل اکسنده یا کاهنده اند که به جای حساس بودن به تغییر غلظت، نسبت به تغییر پتانسیل سیستم جواب می دهند. به این دلیل در عمل به جای تابع P مانند pH، پتانسیل الکترود سیستم را در محور yهای منحنی برای یک تیتراسیون اکسایش-کاهش رسم می کنند. این پتانسیل E از معادله ی نرنست به دست می آید.
فرم و شکل کلی منحنی تیتراسیونهای اکسایش-کاهش با تیتراسیونهای خنثی شدن تفاوتی ندارد.
معادله زیر (در محلول بازی) را موازنه کنید.
ب) برای موازنه کردن H، مانند محلول اسیدی، H+ اضافه می کنیم. با وجود این، چون محلول بازی است، یون های H+ با یون های OH- واکنش می دهند و H2O تولید می کنند. از این رو، در این روش ابتدا برای موازنه کردن H باید H+ اضافه کنیم. H+ با OH- واکنش داده و H2O تولید می کند، سپس دو معادله به دست آمده را با یکدیگر جمع می کنیم.
ج)
مرحله3:
هم ارزها در فرایندهای اکسایش-کاهش
یک هم ارز اسید با یک هم ارز باز واکنش می دهد. به طور کلی این رهیافت در بررسی استوکیومتری واکنش های اکسایش-کاهش و به ویژه الکترولیز نیز مفید است. در یک واکنش اکسایش-کاهش یا الکترولیز، تعدادی الکترون از یک گونه شیمیایی به گونه دیگر انتقال می یابد.جرم یک هم ارز از گونه شرکت کننده در فرایند برابر با جرم یک مول از آن تقسیم بر تعداد الکترون هایی است که به ازای هر مول از آن ماده منتقل می شود. مثلا، در فرایند زیر
دو الکترون به ازای هر مول Zn(s)انتقال می یابد، وزن هم ارز Zn(s) برابر است با 65.4/2=32.7 و یک مول Zn(s) معادل با دو هم ارز می باشد. با وجود این، یک الکترون به ازای هر مول Ag+ منتقل می شود و بنابراین، جرم یک هم ارز از آن مساوی با جرم یک مول از آن و برابر 107.9g است.
تعداد الکترون هایی را که در یک واکنش منتقل می شود غالبا نمی توان با بررسی اجمالی واکنش کلی معلوم کرد. مثلا،
در این جا تعداد الکترون های انتقال یافته را می توان با تقسیم واکنش کلی به دو نیم واکنش تعیین کرد:
با مشاهده نیم واکنش ها در می یابیم که پنج الکترون به ازای یک مول MnO4- منتقل می شود، بنابراین، یک مول MnO4- معادل با پنج هم ارز می باشد. همچنین دو الکترون به ازای هر مول H2SO3 انتقال می یابد، پس یک مول H2SO3 معادل با دو هم ارز است. توجه کنید که در واکنش کلی دو مول یا 10 هم ارز MnO4- با پنج مول یا 10 هم ارز H2SO3 واکنش می دهد.
رابطه بین مول و هم ارز را می توان با محاسبه اعداد اکسایش اتم های گونه های شرکت کننده در فرایند اکسایش-کاهش نیز تعیین کرد. در هر واکنش اکسایش-کاهش، وزن هم ارز یک ماده برابر با وزن فرمولی آن تقسیم بر تغییر عدد اکسایش اتم های تشکیل دهنده آن می باشد. بنابراین هنگامی که MnO4- واکنش داده، Mn2+ و H2O را تشکیل می دهد، عدد اکسایش Mn از 7+ در MnO4- به 2+ در Mn2+ کاهش می یابد، یعنی 5 درجه تغییر می کند. چون عدد اکسایش O تغییر نمی کند، پس وزن هم ارز MnO4- برابر با 1/5 وزن فرمولی آن است.
می توانیم غلظت محلول یک رابطه کاهنده یا یک رابط اکسنده را برحسب هم ارزها با مقایسه مولاریته بیان کنیم. مولاریته (M) یک محلول، مقدار ماده حل شده (برحسب مول) در یک لیتر محلول است. نرمالیته (N) یک محلول، مقدار ماده حل شده (برحسب هم ارز) در یک لیتر محلول است.
مثال:
در واکنش زیر، چند هم ارز KMnO4 برای واکنش با 30 گرم FeSO4 لازم است؟
بنابراین 0/20 هم ارز از KMnO4 لازم می باشد.
مثال:
غلظت محلول KMnO4 0.100 N (برحسب گرم در لیتر) در واکنش زیر چقدر است؟
غلظت = 3/16 گرم بر لیتر
گرم 3/16 = 0/100 هم ارز
منبع:
www.shimihome.com
حل مسائل اکسایش-کاهش 1
مرکز یادگیری سایت تبیان- مرجان سلیمانیان