ید
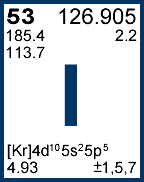
خصوصیات قابل توجه
ید عنصر جامد درخشانی است به رنگ آبی مایل به سیاه که در دماهای استاندارد به بخاری بنفش رنگ و بد بو تبدیل می گردد. این هالوژن همچنین با بسیاری از عناصر، ترکیباتی را می سازد اما از سایر عناصر گروه هالوژن ها فعالیت کمتری داشته و دارای خصوصیاتی شبیه فلزات است. ید به راحتی در کلروفرم، تتراکلرید کربن یا دی سولفید کربن حل شده و محلول های ارغوانی رنگی به وجود می آورد (تنها به مقدار کمی در آب قابل حل است). رنگ آبی سیر با محلول نشاسته ویژگی ید آزاد می باشد.
کاربردها
در مناطقی که غذای آن ها حاوی مقدار کم ید می باشد مثلاً مناطق دور افتاده از دریا که هیچگونه غذای دریایی مصرف نمی شود- کمبود ید ابتلا به بیماری گواتر اصطلاحاً گواتر محلی را افزایش می دهد. در بیشتر (نه تمامی) این مناطق با افزودن مقدار کم یدید سدیم به نمک طعام از ابتلا به این بیماری جلوگیری شده است. این محصول به نام نمک ید دار نیز معروف است.
کاربردهای دیگر این عنصر:
- یکی از هالوژن ها است که وجود آن به مقدار کم برای موجودات زنده حیاتی است ؛ هورمون تیروئید تیروکسین و تری یدوتیرونین حاوی اتم های ید می باشد.
- تنتور ید (3% ید عنصری در پایه آب/اتانول) از اجزاء مهم تمامی وسایل کمک های اولیه می باشد که هم برای ضد عفونی کردن زخم ها و هم برای پاکسازی آب های شرب سطحی مورد استفاده قرار می گیرد (3 قطره در هر لیتر، پس از 30 دقیقه تأثیر می کند).

- ترکیبات ید در رشته شیمی آلی مهم و در پزشکی بسیار سودمند هستند.
- از یدیدها و تیروکسین که حاوی ید هستند در پزشکی داخلی و در ترکیب با الکل (به عنوان تنتور ید) برای ضد عفونی نمودن زخم های بیرونی استفاده می شود.
- یدید پتاسیم در عکاسی کاربرد دارد.
- یدید تنگستن برای تقویت افروزه لامپ ها مورد استفاده قرار می گیرد.
- تری یدید نیتروژن برای کاربردهای تجاری بسیار انفجاری و ناپایدار است اما جزو شوخی های معمول دانشگاهی به حساب می آید.
تاریخچه
ید (واژه یونانِ iodes به معنی بنفش) در سال 1811 توسط Barnard Courtois کشف شد.
پیدایش
ید بسیار خالص را می توان از واکنش یدید پتاسیم با سولفات مس تهیه کرد. البته روش های دیگری نیز برای جداسازی این عنصر وجود دارد.
ایزوتوپ ها
برای ید 30 ایزوتوپ وجود دارد که تنها یکی از آن ها I-127 پایدار است. از ایزوتوپ رادیواکتیو مصنوعی I-131 ( ساطع کننده بتا) که دارای نیمه عمر 8 روز است برای درمان سرطان و دیگر بیماری های غده تیروئید استفاده می گردد. معمول ترین ترکیبات ید عبارتند از یدیدهای سدیم و پتاسیم ( KI) و یدیتها ( KIO3).
ید فقط یک ایزوتوپ پایدار I-127 دارد. با این همه ایزوتوپ های رادیواکتیو ید کاربردهای وسیعی دارند. I-129 با نیمه عمر 17 میلیون سال محصولی از پراش Xe-129 در اتمسفر است اما نتیجه فروپاشی U-238 نیز می باشد.
چون U-238 در خلال فعالیت های مربوط به انرژی هسته ای تولید می شود، وجود آن (به نسبت I-129/I) می تواند فعالیت های در حال انجام در هر مکان را مشخص کند. به همین علت از I-129 در مطالعات آب باران بعد از حادثه چرنوبیل استفاده شد.
از آن همچنین به عنوان ردیاب آب های زیر زمینی و نشان دهنده پراکندگی فضولات در محیط زیست استفاده می گردد. سایر کاربردها ممکن است به وسیله تولید I-129 در پوسته زمین ازطریق تعدادی مکانیسم فروپاشی مختل شود.
I-129 از جهات زیادی شبیه Cl-36|chlorine است. این ایزوتوپ، هالوژنی قابل حل و نسبتاً واکنش ناپذیر است که بیشتر به صورت آنیونی non-sorbing یافت شده و به وسیله واکنش های کیهانزاد، حرارت اتمی و ثابت تولید می شود. در مطالعات آب شناسی چگالی های I-129 معمولاً به نسبت I-129 به مقدار کلی I گزارش می شود (که عملاً I-127 است).
چون نسبت های Cl-36/Cl,I-129/I در طبیعت تقریباً کم می باشد ( 14-10تا 10-10) اوج حرارت اتمی I-129/I در طول دهه 70 و 80 تقریباً به 7-10رسید. I-129 با Cl-36 در بعضی موارد فرق دارد؛ نیمه عمر آن طولانی تر است ( vs6/1 ،3/0 میلیون سال)، به شدت biophilic است و به اشکال یونی چندگانه وجود دارد ( معمولاً I- و یودیت) که دارای رفتار شیمیایی متفاوتی هستند.
هشدارها
تماس مستقیم آن با پوست ممکن است آسیب هایی را به همراه داشته باشد پس هنگام کار با ید باید بسیار احتیاط نمود. بخار ید باعث دردناک شدن چشم و غشاء مخاطی می شود. حداکثر مقدار مجاز ید در هوا نباید از 1 میلی گرم در هر متر مکعب فراتر رود.
مرکز یادگیری سایت تبیان - تنظیم: مریم فروزان کیا

















