
جنبه های بیوشیمیایی تثبیت نیتروژن
اهداف:
- آشنایی با جنبه های بیوشیمیایی تثبیت نیتروژن
- آشنایی با آنزیم های دخیل در این واکنش
شرح درس:
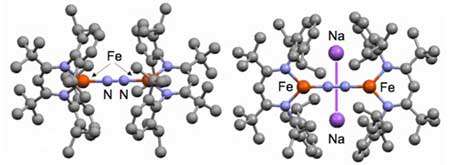
از آنجا که پیوند بین دو اتم نیتروژن بسیار پایدار است، نیتروژن مولکولی به راحتی احیا نمی شود. در فرایند صنعتی مربوطه، احیای باند سه گانه ی نیتروژن مولکولی توسط هیدروژن فقط در دما و فشار بالا مقدور بوده و نیازمند مصرف انرژی نسبتاً زیادی است. احیای بیولوژیکی نیتروژن مولکولی نیز نیازمند همین مقدار انرژی است که این انرژی با مصرف مقدار زیادی از مواد فتوسنتزی گیاه تامین می شود. آنزیم های متعددی در فرایند تثبیت نیتروژن نقش دارند که از آن جمله می توان به آنزیم دی نیتروژناز اشاره نمود.
آنزیم دی نیتروژناز dinitrogenase
تثبیت نیتروژن به وسیله ی یک کمپلکس آنزیمی به نام دی نیتروژناز کاتالیز می شود. تنها پروکاریوت ها قادرند نیتروژن مولکولی را تثبیت کنند، چرا که تنها این سلول ها دارای ژن کد کننده ی آنزیم فوق هستند. آنزیم دی نیتروژناز از تمامی پروکاریوت هایی که نیتروژن را تثبیت می کنند جداسازی شده است.
این آنزیم یک کمپلکس پروتئینی مولتی مریک است که از دو پروتئین با اندازه های متفاوت به وجود آمده است. پروتئین کوچک تر دایمری متشکل از دو زیر واحد پلی پپتیدی یکسان است. جرم مولکولی هر زیر واحد بسته به گونه ی باکتری از 24 تا 36 کیلودالتون است. از آنجاکه این دایمر دارای دسته ای متشکل از چهار یون آهن است که با چهار گروه سولفور پیوند دارند Fe4s4 به آن پروتئین آهن دار گفته می شود. به پروتئین بزرگتر در کمپلکس دی نیتروژناز، پروتئین آهن- مولیبدن گفته می شود. این پروتئین یک تترامر است که از دو جفت زیر واحد یکسان تشکیل شده است و جرم مولکولی 220 کیلودالتون است. هر پروتئین آهن – مولیبدن حاوی دو یون مولیبدن به شکل یک کوفاکتور آهن- مولیبدن- سولفور است.
این پروتئین همچنین حاوی دسته های Fe4s4 است که عدد دقیق آن ها هنوز روشن نشده است. تعداد این دسته ها تابع گونه و همچنین وضعیت فیزیولوژیکی گونه است. معادله ی کلی برای احیای نیتروژن مولکولی به آمونیاک به وسیله ی آنزیم دی نیتروژناز را می توان به صورت زیر نشان داد:
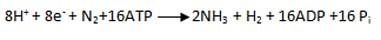
همان گونه که دیده می شود، محصول اصلی تثبیت بیولوژیکی، نیتروژن آمونیاکی است، ولی به ازای هر نیتروژن مولکولی که احیا می شود یک مولکول هیدروژن تولید می شود.
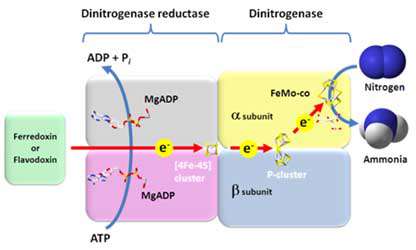
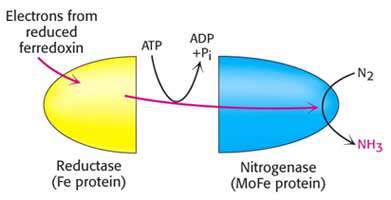
احیای نیتروژن مولکولی، فرایندی دو مرحله ای است. در مرحله ی اول آن پروتئین آهن دار به وسیله ی یک دهنده ی الکترون اولیه که معمولاً فرودکسین ferredoxin است احیا می شود. فرودکسین پروتئینی کوچک با جرم مولکولی 14تا 24 کیلو دالتون است که حاوی یک گروه آهن – سولفور است. الکترون ها توسط جزء آهن که در یکی از دو وضعیت احیا شده فرو Fe2+ یا اکسید فریک Fe3+ وجود دارد حمل می شوند. جالب آنکه فرودکسین نه تنها در تثبیت نیتروژن شرکت دارد،بلکه یک ناقل الکترون مهم درفتوسنتز نیز محسوب می شود. در مرحله ی دوم، شکل احیا شده پروتئین آهن دار الکترون ها را به پروتئین آهن – مولیبدن که احیای گاز نیتروژن مولکولی و همچنین احیای هیدروژن را کاتالیز می کند تحویل می دهد.
جهت دریافت فایل آموزشی کلیک کنید.
نقش ATP در واکنش هنوز به طور دقیق روشن نشده است ولی مشخص شده است که ATP با شکل احیا شده ی پروتئین آهن دار واکنش می دهد. احتمال می رود که ATP در انتقال الکترون ها بین پروتئین آهن دار و پروتئین آهن – مولیبدن ایفای نقش می کند.
مرکز یادگیری سایت تبیان
تهیه: فاضل صحرا نشین سامانی

















