کلسیم
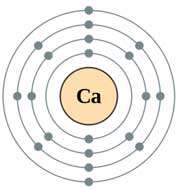
کلسیم عنصر شیمیایی است که با نشان Ca و عدد اتمی 20 در جدول تناوبی وجود دارد. کلسیم فلز قلیایی خاکی نرم و خاکستری رنگی است که در استخراج توریم، زیرکونیم و اورانیوم بعنوان عامل کاهنده به کار می رود. همچنین این عنصر پنجمین عنصر فراوان موجود در پوسته زمین است. وجود این عنصر برای حیات بافت های زنده- به خصوص در فیزیولوژی سلول- ضروری است.
ویژگی های قابل توجه
کلسیم عنصر نسبتاً سختی است که بوسیله الکترولیز از فلورید کلسیم به صورت خالص در می آید و با شعله زرد و قرمز رنگ می سوزد و در معرض هوا لایه نیترید سفید رنگی تولید می کند. این عنصر با آب واکنش داده و پس از جابجایی هیدروژن تولید هیدروکسید کلسیم می کند.
کاربردها
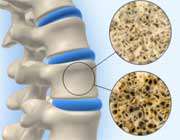
کلسیم عضو مهمی از یک رژیم غذایی سالم است. کمبود جزئی آن برشکل گیری دندان ها و استخوان تاثیر می گذارد و زیادی آن نیز می تواند به سنگ کلیه منجر گردد. برای جذب کلسیم به ویتامین D نیاز است . محصولات لبنی یکی از منابع غنی این عنصر می باشد.
برای اطلاعات بیشتر درمورد نقش کلسیم در موجودات زنده به «Ca«biology مراجعه کنید.
سایر کاربردهای آن عبارتند از:
عامل کاهنده در استخراج سایر فلزات مثل اورانیوم، زیرکونیم و توریم.
اکسید زدا، گوگرد زدا یا کربن زدا برای آلیاژهای مختلف آهنی و غیر آهنی .
عامل آلیاژ که برای تولید آلیاژهای آلومینیوم ، بریلیم، مس ، سرب و منیزیم مورد استفاده قرار می گیرد.
تاریخچه
( لاتین calx ، به معنی آهک) از قرن یکم ، رومیان آهک را تهیه و مورد استفاده قرار دادند اما کلسیم تا سال 1808 کشف نشده بود. Sir Humphry Davy بعد از اینکه فهمید با الکترولیز آهک در جیوه و به وسیله Berzelius وPontin می توان ملغمه کلسیم تولید نمود ، موفق به تولید کلسیم خالص شد.
پیدایش
کلسیم پنجمین عنصر فراوان در پوسته زمین ( تشکیل دهنده 3%) و بخش مهمی از برگ ها، استخوان ها، دندان ها و صدف ها می باشد. کلسیم به علت واکنش پذیری شدیدی که با آب و هوا دارد هرگز در طبیعت به صورت مجرد از دیگر عناصر یافت نمی شود ، بجز در موجودات زنده کــــه 2+ Ca نقش کلیدی در فیزیولوژی سلول به عهده دارد.این عنصر فلزی به مقدار زیاد در سنگ آهک، گچ و فلوریت وجود دارد. آپتیت، فلوروفسفات یا کلروفسفات کلسیم است. از الکترولیز کلرید کلسیم مذاب (CaCl2) برای جداسازی کلسیم خالص استفاده می گردد.
جداسازی (* پیگیری):
کاتد: Ca2+* + 2e- --> Ca
آند: Cl-* --> ½Cl2 (گاز) + - e
ترکیبات
آهک زنده ( CaO ) در بسیاری از فرآیندهای پالایش کاربرد دارد و با حرارت دادن و افزودن حساب شده آب به سنگ آهک بدست می آید. اگر CaO با شن مخلوط گردد ، سفت شده و به mortar تبدیل می گردد ، و با جذب دی اکسید کربن به plaster تبدیل می شود. در صورتیکه CaO با ترکیبات دیگری مخلوط شود ، بخش مهمی از سیمان پورتلند را می سازد. وقتی آب به سنگ آهک یا سایر سنگ های کربنات حل شدنی تراوش کند باعث از بین رفتن قسمت هایی از این سنگ ها شده و موجب تشکیل غارها، طاقدیس و ناودیس و همچنین آب سخت می شود. دیگر ترکیبات مهم کلسیم : نیترات، سولفید، کلراید، کاربید، سیانامید و هیپوکلریت است.
ایزوتوپ ها
کلسیم دارای 6 ایزوتوپ پایدار است که دو تای آن ها در طبیعت یافت می شوند: Ca-40 پایدار و Ca-41 رادیو اکتیو با نیمه عمر 103000 سال که 97% این عنصر به شکل Ca-40 وجود دارد.Ca-40 یکی از محصولات فروپاشی K-40 است – به همراه Ar-40- درحالیکه در علم زمین شناسی تاریخ یابی با K-Ar شدیداً کاربرد پیدا کرده ، Ca-40 در طبیعت کاربرد خود را در تاریخ گذاری از دست داده است. روش هایی با بهره گیری از طیف سنجی جرمی و رقیق سازی ایزوتوپ double spike برای تاریخ گذاری عمر جو به وجود می آیند Ca-41 در اثر فعل و انفعالات نوترون Ca-40 حاصل می شود.
بیشترین تولید آن در بخش های کم و بیش بالاتر پایه خاک است که شار نوترون های کیهانی به مقدار کافی قوی هستند ، چون Ca-41 به شکل k-41 فروپاشی می شود - یک نشانگر بسیار مهم برای تعیین فاصله زاویه ای سیارات از خورشید- لذا Ca-41 در مطالعات نجومی بسیار مورد توجه می باشد.
مرکز یادگیری سایت تبیان