
درصد تفکیک یونی
چکیده: در این درس با مفهومی با نام درصد تفکیک یونی برای مقایسه تمایل ترکیب های کووالانسی محلول در آب به یونش در هنگام حل شدن، آشنا خواهید شد.
شرح درس:
درصد تفکیک یونی (α) رابطه ای است که برای نشان دادن میزان یونیده شدن ترکیب های کووالانسی در آب استفاده می شود. یونیده شدن واژه ای است که زمانی استفاده می شود که یک ترکیب کووالانسی را در آب حل کنیم. در این حالت ابتدا ماهیت پیوند کووالانسی به یونی تبدیل می شود و سپس یون ها از یکدیگر جدا می شوند. درصد تفکیک یونی با رابطه زیر نشان داده می شود:

نکته: در فرمول درصد تفکیک یونی به جای تعداد مول های تفکیک شده در اسیدها (صورت کسر) می توان تعداد مول های تولید شدهH+ و یا تعداد مول های تولید شده یون منفی اسید را قرار داد. هم چنین در این فرمول صورت و مخرج کسر، هر دو باید مول، یا مولکول و یا غلظت مولار باشند.
مثال: اگر غلظت یون H(aq)+ در محلول ٠/٢ مولار استیک اسید، برابر با 1.9 ×10-3 mol.l-1 باشد، درصد تفکیک اسیدی آن در شرایط آزمایش در این محلول چقدر است؟
حل: طبق نکته ای که در بالا گفته شود غلظتH(aq)+ بیانگر تعداد مول های تفکیک شده می باشد.
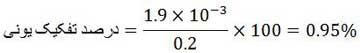
از آنجا که تفکیک یونی به صورت درصد بیان می گردد دامنه تغییرات آن بین ٠ تا ١٠٠متغیر است. در یک تقسیم بندی می توان دامنه تغییرات درصد تفکیک یونی را برای مواد مختلف به این صورت بیان کرد:

در الکترولیت های قوی، درصد تفکیک یونی برابر با 100 یا نزدیک به آن می باشد.

در الکترولیت های ضعیف، درصد تفکیک یونی بین 0 تا 100 بوده و به صفر نزدیکتر می باشد.

در غیرالکترولیت ها، درصد تفکیک یونی برابر صفر است.
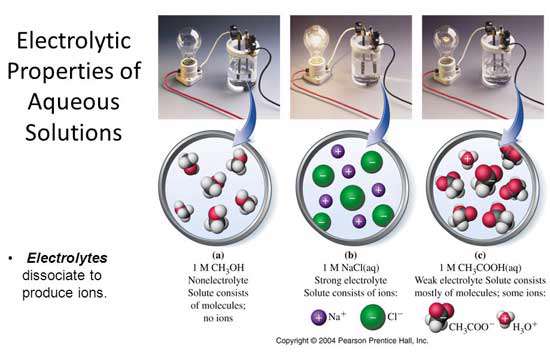
نکته: شرط الکترولیت بودن یک محلول این است که درصد تفکیک یونی در آن بزرگ (نزدیک به ١٠٠) باشد.
نکته: شرط اینکه یک محلول رسانای قوی جریان برق باشد این است که اولا درصد تفکیک یونی آن بزرگ باشد (الکترولیت باشد) و ثانیا انحلال پذیری قابل توجهی داشته باشد.
برخی ترکیب های یونی مانند AgCl و BaSO4 انحلال پذیری ناچیزی دارند. اگرچه مقدار ماده حل شده تقریبا به طور کامل به یون تفکیک می شود و محلول آن ها الکترولیت به حساب می آید، اما تعداد یون های حاصل به اندازه ای نیست که رسانایی قابل توجهی به محلول آن ها بدهد.
درصد تفکیک یونی به دما و غلظت بستگی دارد. با افزایش دما معمولا درصد تفکیک یونی افزایش می یابد زیرا در دمای بالاتر شکسته شدن پیوندها و تشکیل یون ها آسان تر است. اما درصد تفکیک یونی با غلظت رابطه معکوس داشته و با افزایش آن کاهش می یابد. می توان گفت هرچه محلول الکترولیت رقیق تر باشد مقدار درصد تفکیک یونی بیشتر می شود.
مرکز یادگیری سایت تبیان – تهیه و تنظیم: مهسا شاه حسینی

















