
انحلال پذیری گازها در آب
چکیده: فشار، دما و نوع گاز از جمله عواملی هستند که بر انحلال پذیری گازها در آب تاثیرگذارند. در این درس این عوامل را در ارتباط با حلالیت گازها در آب بررسی می کنیم.
شرح درس:
شرایط ایده آل برای انحلال پذیری گازها در آب دمای پایین و فشار زیاد است. در درس قانون هنری به تفصیل پیرامون اثر فشار بر انحلال پذیری گازها صحبت شد و بیان شد که بر طبق قانون هنری انحلال پذیری گازها در آب با فشار رابطه مستقیم دارد.
در مورد اثر دما باید گفت از آنجا که حل شدن گازها در آب با کاهش آنتروپی همراه است به این شرط می تواند خود به خود پیشرفت کند که گرماده باشد. همانطور که از مبحث انرژی آزاد گیبس در فصل ترمودینامیک به یاد دارید، اگر علامت ∆S منفی باشد (نامساعد)، تنها در صورتی واکنش خود به خودی است که عامل تغییر آنتالپی ∆H مساعد بوده و منفی باشد و این امر طبق معادله انرژی آزاد گیبس در دماهای پایین محقق خواهد شد.
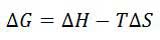
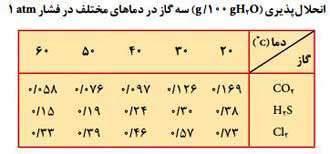
بیشتر بودن میزان انحلال پذیری گاز O2 نسبت به N2 نیز به مرتبه پیوندهای موجود در این دو مولکول مربوط می شود. از آنجا که در مولکول N2 پیوند سه گانه N≡N وجود دارد و نسبت به پیوند دوگانه O=O در مولکول O2 کوتاه تر است، قابلیت جا به جایی ابر الکترونی اتم های آن کمتر بوده و دو قطبی القایی سخت تر ایجاد می شود و جاذبه مولکول های N2 با مولکول های آب کمتر خواهد بود.
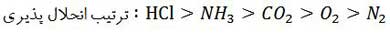
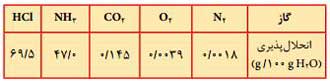
اما اگر دو گاز به مقدار ناچیزی یونیده شوند گازی كه نیروی بین مولكولی و نقطه جوش بیشتری دارد انحلالپذیری بیشتری درآب دارد.
مرکز یادگیری سایت تبیان – تهیه و تنظیم: مهسا شاه حسینی

















