
آنتروپی و آنتالپی انحلال
چکیده:
در فصل ترمودینامیک پیرامون پیش بینی پیشرفت خود به خودی واکنش ها با توجه به علامت ∆H و ∆S بحث شد. حال در این درس به پیش بینی پیشرفت خود به خودی فرایند انحلال از طریق تعیین علامت این دو متغیر تاثیرگذار خواهیم پرداخت.
شرح درس:
آنتروپی و انحلال:
یکی از عوامل بسیار تاثیرگذار در فرایند انحلال تغییر آنتروپی (∆S) است. همان طور که قبلا اشاره شد مواد موجود در جهان هستی میل به بی نظمی بیشتر دارند، در نتیجه آنتروپی بیشتر یک عامل مساعد محسوب می شود. با در نظر گرفتن این اصل به نکات زیر توجه کنید:

انحلال جامد در مایع با افزایش آنتروپی همراه است. ذرات تشکیل دهنده یک جامد بلوری با آرایش منظم کنار هم قرار می گیرند اما ضمن انحلال از این آرایش خارج گشته و میل به بی نظمی و تحرک خواهند داشت.

حل شدن مایع در مایع در جهت افزایش آنتروپی است. زیرا دو مایع که در یکدیگر حل می شوند، حجم بیشتری پیدا می کنند و در یک فضای بزرگ تر تحرک بیشتر و در نتیجه آنتروپی بیشتری خواهند داشت.

حل شدن گاز در مایع با کاهش آنتروپی همراه است. بین ذرات در حالت گازی نیروی جاذبه ضعیفی وجود دارد و بی نظمی زیاد است اما بعد از انحلال گاز در مایع، نیروی جاذبه بین ذره ای افزایش یافته که سبب کاهش تحرک مولکول های گاز و کاهش آنتروپی می شود.
آنتالپی انحلال:
فرایند انحلال با مبادله انرژی همراه است. اگر عمل حل شدن گرماده باشد با کاهش آنتالپی و اگر گرماگیر باشد با افزایش آنتالپی همراه است و هرچه آنتالپی کمتر باشد مساعدتر و هرچه بیشتر باشد نامساعدتر خواهد بود.
موادی که انحلال آن ها در آب گرماده است و در کتاب درسی مطرح شده اند عبارتند از:

اسیدها

بازهای قوی

الکل های سبک، مانند اتانول و متانول

کلیه گازها

CaCl2

فلزهای فعال، اکسید و هیدرید آن ها
نکته: از CaCl2 در بسته های تولیدکننده گرما استفاده می شود زیرا انحلال آن گرماده است. آزمایش ها نشان می دهد که افزودن 40 گرم کلسیم کلرید به 100 میلی لیتر آب 20 درجه سانتیگراد، دمای آب را تا 90 درجه سانتیگراد افزایش می دهد. جالب است بدانید که برای بسته های تولید کننده سرما نیز از انحلال گرماگیر آمونیوم نیترات کمک می گیرند. بسته های تولیدکننده گرما یا سرما در حدود 20 دقیقه کار می کنند. اغلب ورزشکاران برای درمان آسیب دیدگی های خود از این بسته ها استفاده می کنند.


مثال: علامت ∆H و ∆S را در انحلال هر یک از مواد زیر در آب مشخص کنید.
توضیح: در این گونه سوال ها باید توجه داشت که ∆S فقط زمانی منفی است که ماده مورد نظر گازی شکل باشد و ∆H نیز تنها زمانی منفی است که ماده مورد نظر در لیست مواد گرماده موجود در کتاب درسی باشد.
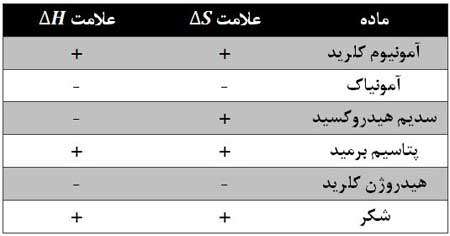
نکته: HCl در حالت گازی، هیدروژن کلرید و در حالت محلول هیدروکلریک اسید نام دارد.
مرکز یادگیری سایت تبیان – تهیه و تنظیم: مهسا شاه حسینی

















