
محاسبه گرمای واکنش به کمک آنتالپی استاندارد تشکیل و آنتالپی پیوند
چکیده: در درس قبل با یکی از روش های غیرمستقیم برای اندازه گیری گرمای واکنش آشنا شدید. در این مطلب دو روش محاسباتی دیگر در تعیین ∆H واکنش ارایه شده است. با توجه به اینکه در مساله چه اطلاعاتی را در اختیار داشته باشیم با استفاده از آنتالپی استاندارد تشکیل و آنتالپی پیوند می توانیم گرمای واکنش را محاسبه کنیم. با ما همراه باشید.
شرح درس:
محاسبه∆H واکنش به کمک آنتالپی های استاندارد تشکیل:
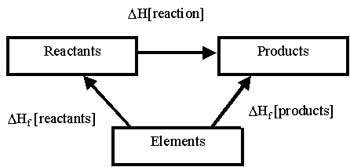
برای محاسبه گرمای واکنش های شیمیایی می توان از آنتالپی استاندارد تشکیل مواد شرکت کننده در واکنش استفاده کرد. البته این روش در صورتی انجام شدنی است که در صورت مساله مقادیر آنتالپی تشکیل واکنش دهنده ها و نیز فراورده ها را در اختیار داشته باشیم. گرمای یک واکنش شیمیایی در دما و فشار ثابت برابر با تفاضل مجموع آنتالپی استاندارد تشکیل فراورده ها (∆Hf2) و آنتالپی استاندارد تشکیل واکنش دهنده ها (∆Hf1) است.
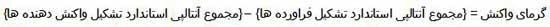
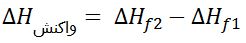
مثال: اگر ∆Ho سوختن اتانول برابر با 1235.3- کیلوژول بر مول باشد، ∆Ho تشکیل آن، چند کیلوژول بر مول است؟ (∆Ho تشکیل CO2(g) و H2O(l) بر حسب کیلوژول بر مول به ترتیب برابر با 393.5- و 242- است.)
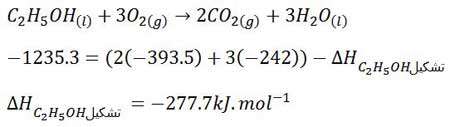
محاسبه ∆H واکنش به کمک آنتالپی های پیوند:
به کمک انرژی پیوند واکنش دهنده ها و انرژی پیوند فراورده ها نیز می توان گرمای یک واکنش را سنجید. در یک واکنش شیمیایی برخی پیوندها در واکنش دهنده ها شکسته شده و پیوندهای جدید در فراورده ها تشکیل می شوند. اگر ∆H واکنش را به تغییرات انرژی پیوندها مربوط بدانیم ، می توانیم از تفاضل انرژی لازم برای شکستن پیوندها (∆HD1 ) و مقدار انرژی آزاد شده پس از تشکیل پیوندها (∆HD2) گرمای واکنش را محاسبه کنیم.

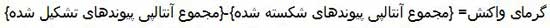
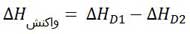
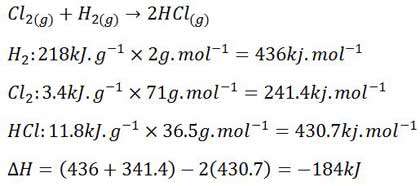
مرکز یادگیری سایت تبیان – تهیه و تنظیم: مهسا شاه حسینی

















