
آنتالپی استاندارد تبخیر، ذوب و تصعید
چکیده: در این درس به تشریح سه مورد دیگر از تغییر آنتالپی های مهم یعنی آنتالپی استاندارد تبخیر، ذوب و تصعید می پردازیم.
شرح درس:
آنتالپی استاندارد تبخیر:
تغییر آنتالپی فرایندی است که طی آن یک مول ماده در دمای جوش خود، از حالت مایع به حالت گاز تبدیل می شود. توجه داشته باشید که آنتالپی استاندارد تبخیر برای تمامی مواد عددی مثبت می باشد زیرا تبخیر فرایندی گرماگیر است.
به عنوان مثال با توجه به واکنش مقابل، آنتالپی استاندارد تبخیر آب، 41.1 کیلوژول بر مول است.
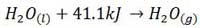

آنتالپی استاندارد ذوب:
تغییر آنتالپی فرایندی است که طی آن یک مول ماده در دمای ذوب خود، از حالت جامد به حالت مایع تبدیل می شود. به عنوان مثال، با توجه به واکنش مقابل، آنتالپی استاندارد ذوب یخ، 6.0 کیلوژول بر مول است.
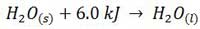
نکته: برای یک ماده معین، آنتالپی تبخیر از آنتالپی ذوب بیش تر است زیرا در عمل ذوب نیروهای بین ذره ای فقط کمی سست می شوند اما در فرایند تبخیر نیروهای بین ذره ای به طور کامل از بین می رود که به گرمای بیشتری نیاز دارد.

آنتالپی استاندارد تصعید:
تغییر آنتالپی فرایندی است که طی آن یک مول از ماده ای از حالت جامد به حالت گاز تبدیل می شود. به عنوان مثال با توجه به واکنش مقابل آنتالپی استاندارد تصعید یخ خشک ( کربن دی اکسید جامد)، 25 کیلوژول بر مول است.
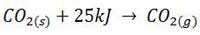
نکته: یخ خشک در فشارهای معمولی به طور مستقیم تصعید می شود.

سوال: آنتالپی تبخیر ید برابر 41.8 kJ.mol-1 و آنتالپی تصعید ید برابر 57.3 kJ.mol-1 است.
آنتالپی ذوب ید بر حسب kJ.mol-1 چند است؟
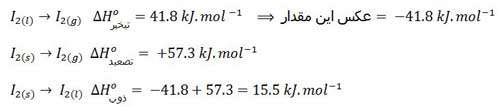
مرکز یادگیری سایت تبیان – تهیه و تنظیم: مهسا شاه حسینی

















