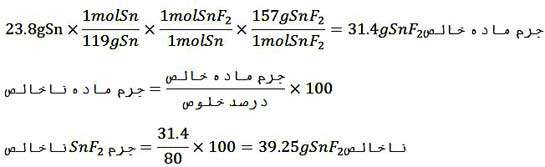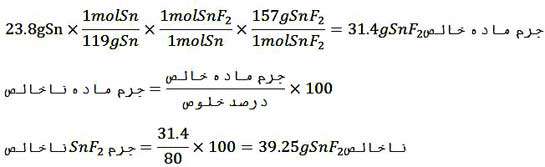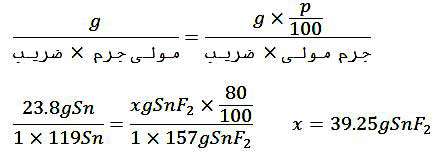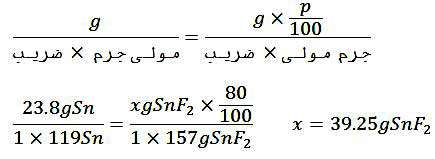درصد خلوص
چکیده:
مواد مورد استفاده در آزمایشگاه یا صنعت کاملا خالص نیستند و معمولا مقادیری مختلفی ناخالصی را به همراه دارند. در این درس به نحوه بدست آوردن درصد خلوص مواد و محاسبه مقادیر مورد نیاز از ماده ناخالص برای شرکت در واکنش های شیمیایی می پردازیم.
شرح درس:
درصد خلوص، مقدار گرم ماده خالص در 100 گرم ماده ناخالص را مشخص می کند. برای مثال در سدیم کلرید ٩٩/٨درصد، از هر 100 گرم سدیم کلرید، ٩٩/٨گرم سدیم کلرید خالص و ٠/٢ گرم ناخالصی وجود دارد. از آنجا که در آزمایشگاه یا صنعت معمولا با مواد کاملا خالص مواجه نیستیم و اغلب مواد، معمولا مقادیر مختلفی ناخالصی را به همراه دارند، برای تامین مقدار معینی از یک ماده خالص همواره باید مقدار بیشتری از ماده ناخالص در دسترس را به کار برد. در مسائلی که صحبت از درصد خلوص می شود از رابطه زیر استفاده می کنیم:
در درس قبل روش تناسب در حل مسائل استوکیومتری معرفی شد. حال اگر بخواهیم برای حل مسائل درصد خلوص از همین روش استفاده کنیم لازم است که مقدار ماده مورد نظر را در P/100 ضرب کنیم که منظور از P همان درصد خلوص است.
مثال: از واکنش ٢٢/٨گرم قلع خالص با مقدار کافی هیدروفلوئوریک اسید، چند گرم قلع (II) فلوئورید با خلوص 80 درصد می توان بدست آورد؟ (F=19، Sn=119)
Sn(s) +2HF(aq) → SnF2(aq) +H2(g)
روش اول – استفاده از ضرایب تبدیل
روش دوم- تناسب