همه چیز درباره متانول
همه چیز درباره متانول
دانش پژوهان عزیز، حتماً تاکنون نام الکل ها را شنیده اید. همان گونه که می دانید، الکل ها دسته ای از ترکیبات شیمیایی هستند که کاربرد های گسترده ای در صنعت دارند. در این بخش می خواهیم شما را با ساده ترین الکل یعنی متانول آشنا سازیم.
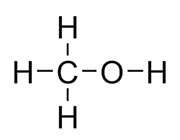
متانول یا متیل الکل واژه ای است که ریشه یونانی دارد. متانول به نام الکل چوب هم شناخته می شود. متانول یک ترکیب شیمیایی با فرمول CH3OH و سادهترین نوع الکل است. متانول مایعی سبک، فرار، بدون رنگ و قابل اشتعال است.
درسال 1892 از طرف انجمن بین المللی نامگذاری ترکیبات شیمیایی، متیل الکل به متانول تغییر نام یافت. متانول در اثر سوختن در هوا تولید دیاکسید کربن و آب می کند. متانول با شعلهای تقریباً بیرنگ می سوزد. این ترکیب از متابولیسم غیر هوازی گونههای زیادی از باکتری ها تولید می شود. در نتیجه مقدار اندکی از بخار متانول در جو وجود دارد. متانول موجود در اتمسفر بعد از گذشت چند روز توسط اکسیژن و نور خورشید به CO2 اکسید می شود.
CH3OH + 3 O2 → 2 CO2 + 4 H2O
در فرآیند مومیایی کردن در مصر باستان، از مادهای استفاده می شد که حاوی متانول بود و از تجزیه حرارتی چوب به دست میآمد. متانول خالص اولین بار در سال 1661 توسط رابرت بویل از چوب استخراج شد.
در سال 1923 شیمیدان آلمانی "آلوین میتاش" متانول را از گاز سنتز (مخلوطی از CO و H2 که از کک به دست میآید) تولید کرده و اختراعی را در 12 ژانویه سال 1926 به ثبت رساند. این واکنش در شرایط بسیار سختی مانند فشار 1000-300 اتمسفر و دمای حدود 400 درجه سانتیگراد انجام شد. امروزه برای تولید متانول، از کاتالیزگرهای با کارایی موثرتر و بهتر که در فشارهای پایین عمل می کنند استفاده می شود.
تولید متانول:
امروزه گاز سنتز(CO و H2) را تحت تاثیر کاتالیزگری که مخلوطی از مس و اکسید روی و آلومینیوم است، واکنش داده و متانول ایجاد می کنند. این کاتالیزگر اولین بار درسال 1966 توسط کمپانی ICI که شرکت شیمیایی انگلیسی است، استفاده شد. این واکنش در فشار 100-50 اتمسفر و دمای 250 درجه سانتیگراد صورت میگیرد. روش های دیگری نیز برای تولید متانول وجود دارد.
کاربرد:
متانول به عنوان حلال، ضدیخ و در تهیه سایر ترکیبات شیمیایی استفاده می شود. هم چنین متانول به صورت محدود به عنوان سوخت در موتورهایی با سیستم احتراق داخلی استفاده می شود. متانول تولید شده از چوب و سایر ترکیبات آلی را متانول آلی یا بیو الکل مینامند که یک منبع تجدید شدنی برای سوخت است و میتواند جایگزین مشتقات نفت خام شود.
40 درصد از متانول تولیدی برای تهیه فرمالدئید استفاده می شود که آن هم در تهیه پلاستیک، تخته سه لایی ، رنگ و مواد منفجره استفاده می شود. برای تغییر ماهیت اتانول صنعتی و جلوگیری از کاربرد آن به عنوان نوشیدنی، مقداری متانول به آن اضافه می کنند. دی متیل اتر از مشتقات متانول است که به جای CFC ها در افشانههای آئروسل به عنوان پیشرانه استفاده می شود.
نکات ایمنی:
متانول ترکیبی سمی است. محصول متابولیت آن، اسید فرمیک و فرمالدئید، سبب نابینایی و مرگ می شود. متانول از طریق نوشیدن، تنفس و جذب از راه پوست وارد بدن می شود. به طور مداوم در معرض آن بودن و استفاده از آن بدون محافظ (ماسک و دستکش) خطرناک است.
در صورت نوشیدن آن بلافاصله باید با پزشک تماس گرفته شود. اثرات سمی متانول چند ساعت بعد از مصرف شروع می شود. بنابراین استفاده سریع از پاد زهر مناسب می تواند از بروز آسیب های دایمی جلوگیری کند. دوز کشنده متانول، 100-125 میلی لیتر است. یکی از پاد زهرهای متانول، استفاده از اتانول می باشد که به آهستگی متانول را در کبد تجزیه می کند. نشانههای نوشیدن متانول شامل سردرد، سرگیجه، تهوع، عدم تعادل، پریشانی، خواب آلودگی و سرانجام بیهوشی و مرگ است.
مطالب مرتبط:
رابطه بین مول و مواد مرکب در شیمی
بخش پژوهش های دانش آموزی تبیان، تهیه: نفیسه مدانلو
تنظیم: نسرین صادقی






















