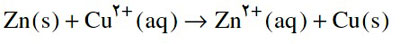سلول های الکتروشیمیایی گالوانی
چکیده:
گروهی از سلول های الکتروشیمیایی گالوانی یا ولتایی هستند که در این جا با نحوه ی کار و انواع آن ها آشنا خواهیم شد.
شرح درس:
سلول گالوانی:
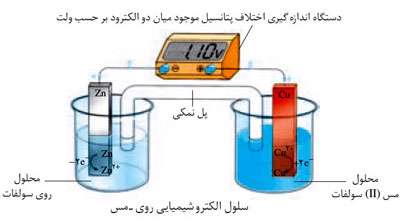
سول الکتروشیمیایی گالوانی یا ولتایی دستگاهی است که انرژی شیمیایی را به انرژی الکتریکی تبدیل می کند و در واقع به کمک واکنش های شیمیایی، جریان برق تولید می کند. از اتصال دو نیم سلول یک سلول الکتروشیمیایی گالوانی ساخته می شود. برای مثال سلول الکتروشیمیایی (Zn-Cu) از دو نیم سلول روی و مس تشکیل شده است.
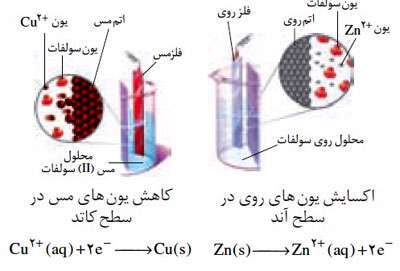
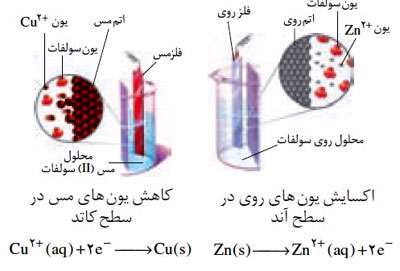
در سلول الکتروشیمیایی(Zn-Cu) ، از آنجایی که نیم سلول رویE° کوچکتری دارد تمایل بیشتری برای دادن الکترون داشته و الکترون ها از آن خارج شده و به سمت الکترود مس حرکت می کنند. خروج الکترون ها از نیم سلول روی باعث می شود تا تعادلی که قبلا در این نیم سلول برقرار بود، یعنی تعادل Zn2+(aq) + 2e- <---> Zn(s) به هم بخورد و طبقاصل لوشاتلیه در جهت برگشت یعنی در جهت اکسایش پیش برود تا کمبود الکترون های خارج شده در آن جبران شود. در اثر این جابه جایی اتم های روی به یون هایZn2+(aq) تبدیل می شوند و به مرور جرم تیغه ی روی کاهش می یابد.
با ورود الکترون ها به الکترود مس تعادلی که قبلا در این الکترود برقرار بود یعنی تعادل Cu2+(aq)+ 2e- <---> Cu(s) به هم خورده و طبق اصل لوشاتلیه برای مصرف الکترون های وارد شده در جهت رفت یعنی در جهت کاهش پیش می رود. در اثر این جابه جایی کاتیون های Cu2+(aq) با جذب الکترون ها از سطح تیغه تبدیل به اتم های Cu می شوند و جرم تیغه ی مس افزایش می یابد. حال با توجه به این توضیحات باید بدانید که الکترودی که E° منفی تری دارد اکسایش می یابد و الکترودی که E° مثبت تری دارد کاهش می یابد.
آند الکترودی است که در آن عمل اکسایش انجام می شود و در آن از رسانای یونی به رسانای الکترونی، الکترون داده می شود.
کاتد الکترودی است که در آن عمل کاهش صورت می گیرد و در آن از رسانای الکترونی به رسانای یونی، الکترون داده می شود.
قطب منفی الکترودی است که تراکم نسبی الکترون در سطح آن بیش تر بوده و E° منفی تری دارد.
قطب مثبت الکترودی است که تراکم نسبی الکترون در سطح آن کمتر بوده و E° مثبت تری دارد.
با توجه به تعاریف بالا در سلول شیمیایی (Zn-Cu) ، نیم سلول روی نقش آند را داشته و قطب منفی است. هم چنین نیم سلول مس نقش کاتد را داشته و قطب مثبت است .
توجه: علامت های + و – ربطی به نامگذاری الکترودها به صورت آند و کاتد ندارند.
نکته: در سلول الکتروشیمیایی گالوانی جهت حرکت الکترون ها از آند به طرف کاتد است.
واکنش کلی سلول گالوانی:
واکنش کلی سلول الکتروشیمیایی (Zn-Cu) به این صورت است :
برای نوشتن واکنش کلی هر سلول گالوانی ابتدا ب کمک جدول E° ، آند و کاتد را مشخص کرده و واکنش را بر اساس فرم کلی زیر می نویسیم:
محاسبه ی E° سلول:
برای محاسبه ی E° سلول یا همان نیروی الکتروموتوری که در مطالب قبل به آن اشاره شد، از رابطه ی زیر استفاده می کنیم:
E°سلول = E° کاتد + E° آند
مثال: نیروی الکتروموتوری سلول الکتروشیمیایی (Zn-Cu) به این صورت محاسبه می شود:
E°سلول = E° کاتد - E° آند =E(Cu2+/Cu) – E(Zn2+/Zn) = +0.34 – ( -0.76) = +1.10v
انواع سلول های گالوانی :
سلول های گالوانی منبع انرژی الکتروشیمیایی هستند و به دو دسته ی نوع اول و نوع دوم تقسیم می شوند. سلول های نوع اول غیر قابل شارژ بوده و با تمام شدن واکنش دهنده های موجود در آن ها غیر فعال می شوند. سلول های سوختی و باتری های خشک از جمله سلول های نوع اول هستند. از انواع باتری های خشک می توان باتری لکلانشه و باتری قلیایی را نام برد.
سلول های نوع دوم را می توان بارها شارژ کرد و مورد استفاده قرار داد. سلول های نوع دوم شامل سلول های انباره ای (مانند: باتری خودرو) و باتری های قابل شارژ ( مانند: باتری نیکل، کادمیم که در تلفن همراه ، تلفن بی سیم، ماشین های اصلاح و لپ تاپ استفاده می شود) است.