
تعیین عدد اکسایش با روش تشکیل معادله
در مطلب قبل با مفهوم عدد اکسایش و استفاده از ساختار الکترون - نقطهای ترکیب برای تعیین عدد اکسایش هر اتم آشنا شدید. در این جا قواعد مربوط به روش دوم در تعیین عدد اکسایش یعنی استفاده از معادله را با هم مرور خواهیم کرد.

درتعیین عدد اکسایش بدون استفاده از رسم ساختار الکترون - نقطهای و با تشکیل معادله قواعدی به شرح زیر وجود دارد:
1ـ عدد اکسایش عنصرها در حالت آزاد برابر صفر است. مانند: H2 ، Cu، Li و...
2ـ عدد اکسایش اکسیژن معمولا برابر 1+ است.اما در هیدرید های فلزی عدد اکسایش آن برابر 1ـ است.هیدریدها ترکیباتی دارای یون هیدرید (H- ) هستند مانند: KH
3ـ عدد اکسایش اکسیژن معمولا برابر 2ـ است. اما درH2O2، HOF، OF2 و O2F2 و... به ترتیب برابر 1+ ، 2+ ،صفر، 1- است. بد نیست بدانید که در یون O+2 که دیوکسیژنیل نام دارد عدد اکسایش اکسیژن برابر (+1)/2 است هم چنین در سوپراکسیها مانند KO2 ، عدد اکسایش اکسیژن(-1)/2 است.
4ـ عدد اکسایش فلزات همواره مثبت و برابر ظرفیت آن هاست. برای مثال در Fe2(SO4)3، ظرفیت آهن برابر 3 است پس عدد اکسایش آن نیز برابر 3+ میباشد.
5ـ عدد اکسایش یونهای تک اتمی برابر بار یون است. برای مثال عدد اکسایش مس در Cu+ برابر 1+ است.
6ـ عدد اکسایش فلوئور در ترکیبها همواره برابر 1ـ است. زیرا فلوئور الکترونگاتیوترین عنصر است. دقت داشته باشید که عدد اکسایش فلوئور در حالت آزاد (F2) مانند دیگر عناصر برابر صفر است.
7ـ دیگر هالوژنها (CL، Br، I ) در ترکیب با عناصری که الکترونگاتیوی کمتری نسبت به آن ها دارند و یا الکتروپوزتیوتر هستند عدداکسایش 1ـ دارند.
8ـ مجموع عدد اکسایش عنصرها در یک مولکول برابر صفر و در یک یون برابر بار یون است.
9ـ در بین عناصر، گروهی وجود دارند که همیشه در ترکیبهای خود فقط یک نوع عدد اکسایش دارند این عناصر به همراه عدد اکسایش آن ها به شرح زیر هستند:
فلزهای گروه یک=1+
فلزهای گروه دو=2+
فلوئور=1ـ
آلومینیوم=3+
اسکاندیم=3+
روی=2+
نقره=1+
مثال: در ترکیبهای زیر عدد اکسایش اتمهایی که زیر آن ها خط کشیده شده است را تعیین کنید؟
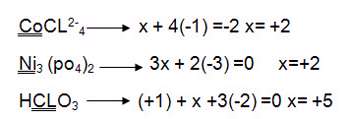
نکته: برای تشکیل معادله در ترکیباتی که دارای یونهای چند اتمی هستند، بار یون چند اتمی را قرار میدهیم.

















