ترکیبات مولکولی
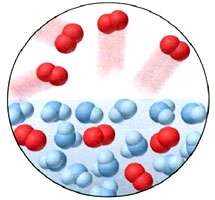
اتمها عمدتاً توسط یک نیروی پیوندی در کنار یکدیگر قرار میگیرند و تشکیل مولکول و ترکیبات مولکولی میدهند. نوع پیوند و قدرت آن میتواند متغیر باشد. در این بخش ترکیبات مولکولی را بررسی میکنیم.
هر مولکول، ذرهی سازندهی مادهای است که به آن ترکیب مولکولی میگویند. ترکیبات مولکولی حاصل ایجاد پیوند کوالانسی (اشتراکی ) بین نافلزات است و فراوانترین ترکیب مولکولی در طبیعت آب است. از میان ترکیبات مولکولی اشاره شده در کتاب میتوان این ترکیبات را نام برد.
یک مولکول، مجموعهای از اتمهای یک مادهی مشخص دارای فرمول شیمیایی است. کلمهی مولکول از زبان لاتین گرفته شده و به معنی تودهی کوچکی از مواد میباشد. برای مثال مولکول متان، از یک اتم کربن و چهار اتم هیدروژن تشکیل شده است یایک مولکول آب از یک اتم اکسیژن و دو اتم هیدروژن تشکیل شده است. یک مولکول ذرهای است که دارای قابلیت حرکت و مستعد دادن واکنش شیمیایی با مواد دیگر است، در حالی که اتم از ذرات کوچک ثابتتری تشکیل شده و جابهجایی آنها نیازمند انرژی بسیار زیادی است که برای انجام واکنشهای هستهای ضروری است.
مولکولهای یک ماده در حال جنبش و حرکت دائمی هستند. این جنبش مولکولها حرکت براونی نام دارد که برای اولین بار توسط روبرت براون در سال 1821 میلادی کشف شده است. وقتی ماده به شکل گاز است مولکولها دارای جنبش بسیار زیاد هستند و فضای بین مولکولها زیاد است. در حالت مایع فضای بین مولکولی کمتر و جنبش مولکولها نیز کمتر است. در حالت جامد مولکولها به صورت منظم چیده شدهاند و دارای چرخش به دور یک فضای مشخص هستند. دمای یک ماده نشانگر میزان جنبش مولکولهای آن ماده است.
ترکیبات کووالانسی
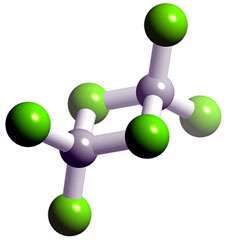
گاه اتمها برای رسیدن به آرایش گاز نجیب (آرایش هشتایی) به جای از دست دادن یا گرفتن الکترون آنها را میان خود به اشتراک میگذارند. در این حالت میان دو اتم پیوندی به وجود میآید که به آن پیوند کووالانسی میگویند. به عنوان مثال ترکیبی مانند ید که از به اشتراک گذاشته شدن زوج الکترون پیوندی میان دو اتم حاصل شده است. به چنین ترکیبهایی که از مولکولهای جدا از هم تشکیل شدهاند، ترکیبهای مولکولی میگویند.
پیوند کووالانسی نتیجه تأثیر نیروهای جاذبهای و دافعهای بر یکدیگر است. مثلاً در H2 با نزدیک شدن اتمهای هیدروژن به هم میان الکترونهای یک اتم و هسته اتم دیگر نیروی جاذبه و میان الکترونهای یک اتم و الکترونهای اتم دیگر و همچنین میان هستههای آنها نیروی
دافعه به وجود میآید. اما در هنگام تشکیل پیوند کووالانس اثر نیروی جاذبه بیشتر است و در نتیجه پیوند تشکیل میشود. پس از تشکیل پیوند نیروهای جاذبه و دافعه برابر شده و اتمها در فاصله تعادلی نسبت به هم قرار میگیرند.

پیوند داتیو
پیوند داتیو هنگامی به وجود میآید که دو اتم تشکیل دهندهی پیوند یکی دست کم دارای یک جفت الکترون ناپیوندی و دیگری دارای دست کم یک اوربیتال خالی باشد مانند کاتیون آمونیوم که از اتصال یک مولکول آمونیاک و یک یون هیدروژن به وجود میآید.
مرکز یادگیری سایت تبیان - تهیه: مرتضی عرفانیان
تنظیم: مریم فروزان کیا

















