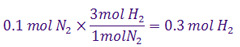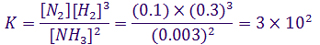مسائل ثابت تعادل
در ادامه معرفی رابطه ثابت تعادل و بررسی نکات مربوط به آن، مسائلی در ارتباط با ثابت تعادل مطرح می شود. در اینجا قصد داریم ابتدا مسیر حل این مسائل را مشخص کرده و با ذکر چند مثال به نکات مهمی که ممکن است در حل مسائل با آنها برخورد کنید، بپردازیم.
مطرح شدن غلظت تعادلی:
مثال: مقداری NH3(g) را در ظرف سربسته یک لیتری حرارت می دهیم تا تعادل گازی :
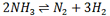
برقرار شود. اگر مقدار N2(g) و NH3(g) در مخلوط به حالت تعادل به ترتیب 0.1 و 0.003 مول باشد، مقدار K در دمای آزمایش کدام است؟
حل:
نکته مهم: هنگامی که غلظت یکی از فراورده ها در مسئله داده نمی شود، می توان آن را با توجه به ضرایب استوکیومتری، به کمک فراورده دیگر، بدست آورد. توجه کنید وقتی ظرف یک لیتری است تعداد مول در واقع همان غلظت مولی را نشان می دهد.
مطرح شدن غلظت اولیه مواد:
وقتی در مسائل مربوط به ثابت تعادل صحبت از غلظت اولیه مواد می شود، ابتدا بهتر است جدولی رسم کنیم و اطلاعات مسئله را در آن وارد کنیم.
واکنش فرضی aA+bB ‡ cC+dD را در نظر بگیرید، در ردیف اول جدول غلظت اولیه (M1) تمامی مواد نوشته می شود. از آنجاییکه معمولا واکنش های تعادلی تنها با مقادیری از مواد واکنش دهنده آغاز می شوند، غلظت های اولیه فراورده ها را صفر در نظر می گیریم مگر آنکه در مسئله غلظت اولیه فراورده ها ذکر شده باشد.
در ردیف دوم جدول تغییر غلظت ها (∆M ) را قرار می دهیم. توجه داشته باشید ضرایب استوکیومتری نسبت تغییر غلظت ها را نشان می دهند. یعنی در واکنش فرضی مورد نظر به ازای مصرف ax مول از ماده A و bx مول از ماده B، cx مول از ماده C و dx مول از ماده D در حال تولید است. علامت تغییر غلظت برای واکنش دهنده ها منفی است، زیرا واکنش دهنده ها در حال مصرف هستند. نهایتا در ردیف سوم جدول غلظت های نهایی یا غلظت های تعادلی (M2) قرار می گیرند. این ردیف حاصل جمع ردیف های قبلی است.
دو نکته:
- در مورد واکنش دهنده ها به مقدار ∆M ، مقدار مصرف شده، یا تجزیه شده یا در واکنش شرکت کرده می گویند. اما در مورد فراورده ها به مقدار ∆M ، مقدار تولید شده می گویند.
- در مورد واکنش دهنده ها به مقدار M2 ، غلظت در حال تعادل یا غلظت تعادلی یا غلظت نهایی یا غلظت باقی مانده یا مقدار واکنش نکرده می گویند. در مورد فراورده ها نیز به مقدار M2 ، غلظت تعادلی یا غلظت در حالت تعادل می گویند.
مثال: مقدار 4.4 مولHI(g) را در ظرف سربسته یک لیتری گرما می دهیم تا تعادل گازی: 2HI ‡ H2+I2 ، برقرار شود. در این حالت 4 مول HI(g) باقی مانده است. مقدار ثابت تعادل (K) در دمای آزمایش کدام است؟
حل:
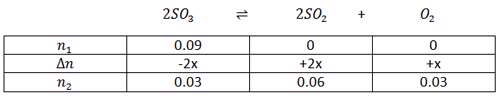
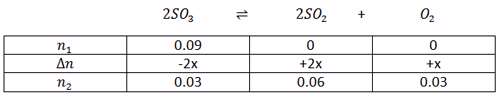
مثال: مقدار 0.09 مول گوگرد دی اکسید را در ظرف سربسته تا رسیدن به تعادل گازی : 2SO3 ‡ 2SO2+O2 ، گرم می کنیم. اگر ثابت تعادل در این شرایط برابر 0.03 و مقدار 0.03 مول گاز O2 در حالت تعادل وجود داشته باشد، حجم ظرف آزمایش چند لیتر است؟
تذکر: اگر حجم ظرف مجهول بوده و یا یک لیتر نبود، هم چنین اگر ماده جامد یا مایع خالص در واکنش داشته باشیم، بهتر است در تنظیم جدول به جای غلظت از تعداد مول ها استفاده کنیم. در رابطه ثابت تعادل مول های تعادلی تقسیم بر حجم ظرف می شود.
سوال: در واکنش تعادلی A+2B ‡ 2C اگر غلظت مولی مواد شرکت کننده به ترتیب[C]=2 و [B]=1 و[A]=0.5 باشد مقدار ثابت تعادل چقدر خواهد بود؟
1- 9
2- 8
3- 6
4- 4