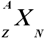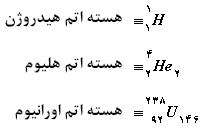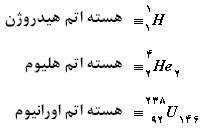ساختار هسته
آیا هسته هم مانند اتم دارای اجزاء كوچكتری است؟ چه نیرویی آن ها را به هم پیوند میدهد؟
در اوایل قرن بیستم، سؤال هایی اساسی برای دانشمندان مطرح شدند.
در آن زمان دانشمندان اتم را شامل یك هسته و الكترون هایی كه در اطراف آن در چرخشند، میدانستند، در ضمن هر اتم از اتم دیگر به خاطر هسته ی متفاوتی كه داشت، متمایز میشد. خواص شیمیایی متفاوت آن ها نیز به مقدار بار الكتریكی هسته بستگی داشت.
به عنوان مثال هیدروژن دارای یك الكترون منفی و یك هسته با بار مثبت است در حالی كه اكسیژن دارای 8 الكترون با بار منفی و هسته ایی با بار 8+ است. اتمها تنها با گسیل الكترون یا دریافت الكترون با مواد اطراف خود ارتباط پیدا میكنند، بنابراین در واكنشهای شیمیایی عنصر عوض نمی شود.
حال برویم سراغ هسته. همان طور كه میدانید اورانیوم از خود ذرّات α گسیل میكند یعنی ذره ای با جرمی چهار برابر جرم هسته هیدروژن. این ذره از كجا آمده است؟ این سۆال جدی و مهمی بود زیرا در اطراف هسته فقط الكترون قرار دارد. آیا این ذره از هسته اتم جدا شده است؟
بدین شكل دانشمندان برای هسته اتم جزء ریزتری در نظر گرفتند. در سال 1243 شمسی (1914 م) رادرفورد چنین ادعا نمود كه: باری كوچكتر از بار الكترون یا بار هسته هیدروژن وجود ندارد. به همین خاطر هسته هیدروژن را پروتون (Poroton) نامید كه واژه ای بر گرفته از یك واژه یونانی به معنی نخست است.
برای هستههای دیگر هم به ازای هر یك بار الكتریكی، یك پروتون در نظر گرفت. اما یك مشكل مهم پیش آمد. به عبارتی جرم هستهها با جرم پروتون هایی كه داشتند برابر نمی شد. به عنوان مثال جرم هسته هلیوم 4 برابر جرم هیدروژن است، در حالی كه بار هسته آن 2 بار مثبت است و طبق قاعده ایی كه رادرفورد گفت باید جرم آن 2 برابر جرم هیدروژن میبود. در هستههای سنگین تر وضع بدتر بود. به عنوان مثال جرم هسته اورانیوم 238 برابر جرم هسته هیدروژن است در حالی كه بار آن 92 مثبت است.
به نظر شما این جرم اضافی از كجا ناشی شده است؟ چه چیزی باعث میشود كه جرم هسته از قاعده رادرفورد تبعیت نكند؟
دانشمندان درون هسته را مورد كاوش قرار دادند تا علت این اختلاف جرم را بیابند. در سال 1311 شمسی (1932 م) "چدویك" دانشمند انگلیسی، جوابی برای آن یافت. در آن زمان اتاقكی به نام اتاقك ابر وجود داشت كه رد و مسیر حركت ذره باردار در آن مشخص میشد زیرا هنگام عبور ذرّات باردار از درون بخار آب، قطرههای ریز آب دور آن ها جمع میشدند و مسیر حركت ذره توسط قطرههای آب به جا مانده و مشخص میشد. در شكل زیر یك اتاق ابر و مسیر ذرّات را در آن میبینید.
بنابراین چدویك هنگام بمباران بریلیوم توسط ذرّات α با ذرّات جدیدی رو به رو شد كه رد آن ها در اتاقك ابر بر جای نمی ماند. پس باید بدون بار الكتریكی باشند. از طرف دیگر جرم آن ها باید نزدیك جرم پروتون باشد چرا كه از هسته پارافین، پروتون جدا میكند. چدویك نام آن را "نوترون" (Neutron) گذاشت كه یك واژه لاتینی به معنی نه مثبت و نه منفی است.
در شكل مقابل اتاقك ابری را میبینید كه محل تولید نوترون با علامت + مشخص شده است.
با فرض وجود نوترون مشكل قاعده رادرفورد حل شد. حال دانشمندان چیزی درون هسته كشف كرده بودند كه جرم هسته را بدون افزایش بار آن، افزایش میداد. بنابراین مشخص شد هسته از دو نوع ذره به نامهای پروتون و نوترون ساخته شده است و جرم آن ها نیز برابر است. به پروتون و نوترون درون هسته نوكلئون میگویند. بنابراین وقتی ذره α از هستهای جدا میشود اتفاق زیر برای آن هسته روی میدهد.
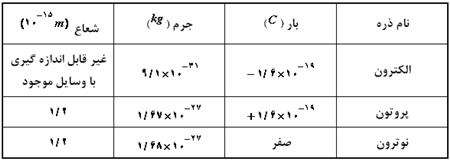
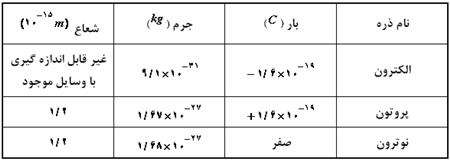
در جدول زیر جرم و بار اجزاء اتم مقایسه شده اند.
تعداد پروتونهای هسته را عدد اتمی میگویند و با Z نشان میدهند. تعداد نوترونهای هسته را عدد نوترونی میگویند و با N نشان میدهد. تعداد كل نوكلئونهای هسته (مجموع پروتون و نوترون) را عدد جرمی میگویند و با A نشان میدهند. بنابراین داریم: A=Z + N
هسته هر اتم را به صورت زیر با قرار دادن A ،Z و N در جای مناسب نشان میدهند.
به عنوان مثال:
مرکز یادگیری سایت تبیان - تهیه: محسنی
تنظیم: مریم فروزان کیا