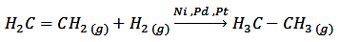واکنش هیدروژن دار کردن اتن و جذب سطحی
در مقالات قبل مفهوم سینتیک شیمیایی، نظریات مربوطه و ساز و کار واکنش های شیمیایی و عوامل موثر بر سرعت واکنش ها مورد بحث و بررسی قرار گرفتند. در آخرین مطلب فصل سینتیک شیمیایی به بررسی واکنش هیدروژن دار کردن اتن می پردازیم و مسایل پیرامون آن را توضیح خواهیم داد تا تمامی مطالب در حوزه ی کتاب درسی شیمی پیش دانشگاهی در این فصل مورد بررسی قرار گرفته باشد.
واکنش هیدروژن دار کردن:
دسته ای از ترکیبات آلی وجود دارند که در ساختار خود دارای پیوند C=C یا C≡C هستند. این ترکیب ها که اصطلاحا سیر نشده خوانده می شوند تمایل دارند که هیدروژن جذب کنند تا در زنجیره کربنی خود تمامی پیوند ها به صورت C-C باشد و تبدیل به ترکیبات سیر شده شوند.
یادآوری: به ترکیبات آلی دارای پیوند C≡C آلکین، دارای پیوند C=C آلکن و دارای پیوند C-C آلکان گفته می شود.
به واکنش افزایش H2 به پیوند دوگانه در ترکیب های آلی سیر نشده و تبدیل آن ها به یک ترکیب سیرشده واکنش هیدروژن دار کردن می گویند.
این واکنش در صنعت نفت برای تبدیل آلکن به آلکان و در صنایع غذایی برای تبدیل روغن های مایع به روغن های جامد کاربرد دارد.
این واکنش در غیاب کاتالیزگر بسیار آهسته انجام می شود ولی در حضور گرد ریز نیکل، پلاتین و یا پالادیم به عنوان کاتالیزگر( گرد ریز کاتالیزگر باعث می شود سطح تماس زیاد شود.)، چه در فشارهای بالای گاز هیدروژن و چه در دمای اتاق سریع انجام می شود.
نکته: واکنش هیدروژن دار کردن در حضور کاتالیزگر از نوع ناهمگن است.
جذب سطحی:
فلزات کاتالیزگر با جذب مواد واکنش دهنده روی سطح خود واکنش هیدروژن دار را کاتالیز می کنند.
در مورد نحوه جذب مولکول های گازی در سطح کاتالیزگر جامد معمولا از نظریه اوربیتال مولکولی استفاده می شود که شرح آن در این مقاله نمی گنجد. اما برای درک بهتر موضوع در همین حد بدانید که اتم های سطح فلز،اوربیتال های اشغال نشده ای دارند که می توانند با الکترون های مولکول های گازی جاذبه برقرار کنند.
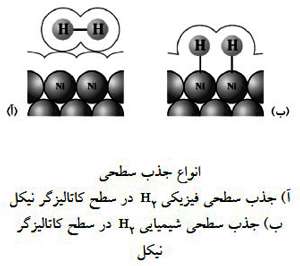
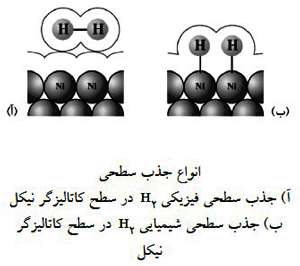
در ضمن بسیاری از فلزهای واسطه اوربیتال های d پر نشده دارند. این اوربیتال های d می توانند برای جذب شیمیایی گازها مورد استفاده قرار گیرند. در واکنش هیدروژن دار کردن اتن با کاتالیزگر نیکل، بر اثر جاذبه ای که بین مولکول های هیدروژن یا اتن یا اتم های سطح فلز Ni به وجود می آید پیوند H-H و C=C سست می شوند و با انرژی فعال سازی کمتری حاضر به شرکت در واکنش می شوند. جذب سطحی در سطح جامد ها به دو صورت فیزیکی و شیمیایی اتفاق می افتد. در جذب فیزیکی فقط نیروی وان دروالسی ایجاد می شود و ماده جذب شونده با سطح جاذب هیچ گونه پیوند شیمیایی ندارد. در جذب شیمیایی ماده جذب شونده با سطح جاذب، پیوند شیمیایی ( مانند کووالانسی) تشکیل می دهد.
تذکر: جذب شیمیایی از جذب فیزیکی قوی تر است.
در هیدروژن دار کردن اتن هر دو نوع جذب فیزیکی و شیمیایی رخ می دهد، به این صورت که مولکول های گازی که بسیار به سطح Ni نزدیک هستند جذب شیمیایی برقرار کرده ولی مولکول های گازی که به نسبت دورترند فقط جذب فیزیکی دارند. در فرآیند کاتالیزی اعتقاد بر این است که جذب فیزیکی اثر مهمی ندارد و نقش اصلی به عهده جذب شیمیایی است.
نکته: در هیدروژن دار شدن هیدروکربن ها بدون حضور کاتالیزگرعامل اصلی که باعث کاهش سرعت می شود پیوند H-H است، زیرا شعاع اتمی هیدروژن بسیار کوچک و در نتیجه طول این پیوند بسیار کوتاه است.
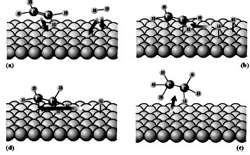
مراحل چهارگانه هیدروژن دار کردن اتن (اتیلن) C2H4 یا H2C=CH2 :
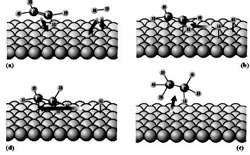
مرحله اول: مولکول های هیدروژن و اتن انتشار می یابند و از محیط واکنش به سطح کاتالیزگر نزدیک می شوند.
مرحله دوم: مولکول های هیدروژن و اتن روی سطح کاتالیزگر جذب شیمیایی می شوند.
مرحله سوم: ابتدا مولکول های اتن و یکی از اتم های هیدروژن ( که همگی در سطح کاتالیزگر جذب شده اند) با یکدیگر واکنش می دهند و رادیکال اتیل و نیز رادیکال هیدروژن را ایجاد می کنند. این رادیکال ها که ذره های فعالی هستند روی سطح کاتالیزگر با ایجاد پیوند شیمیایی جذب می شوند. سپس رادیکال اتیل تولید شده با دومین اتم هیدروژن واکنش می دهد و مولکول اتان (C2H6) را به وجود می آورند.
مرحله چهارم: مولکول اتان تولید شده از سطح کاتالیزگر جدا شده و در محیط واکنش انتشار می یابد.
چند نکته:
مرحله سوم می تواند هفت نام داشته باشد:
1- مصرف اتن
2- تولید اتیل
3- مصرف اتیل
4- تولید اتان
5- تبدیل اتن به اتیل
6- تبدیل اتیل به اتان
7- تبدیل اتن به اتان
اتیل نقش ترکیب واسطه را دارد چون اول تولید و بعد مصرف شده است.
رادیکال ها گونه هایی یک یا چند اتمی هستند که دارای یک یا چند الکترون جفت نشده اند. رادیکال ها گونه های فعالی هستند و به سرعت وارد واکنش می شوند. الکترون ( های) یک رادیکال را با قرار دادن یک نقطه در کنار نماد یا فرمول شیمیایی آن رادیکال نمایش می دهند. برای مثال رادیکال متیل را با نماد .CH3 نشان می دهند.
مرکز یادگیری سایت تبیان- تهیه : مهسا شاه حسینی