
عوامل موثر بر سرعت واکنش های شیمیایی
در این طرح درس دانش آموزان با عوامل موثر بر سرعت شنا خواهیم شد و چهار مورد از این عوامل را با ذکر مثال مورد بررسی قرار خواهیم داد.
عوامل موثر بر سرعت واکنش های شیمیایی:
- ماهیت واکنش دهنده ها
- حالت فیزیکی
- غلظت
- دما
- کاتالیزگر
اثر ماهیت واکنش دهنده ها:
این عامل اگرچه به عنوان یک متغیر در بهبود سرعت واکنش مطرح نیست اما از چهار عامل دیگر مهم تر است. برای مثال اگر در مخلوطی از گازهای H2 و O2 جرقه ای زده شود یک واکنش بسیار سریع همراه با انفجار رخ خواهد داد.
اما زدن همین جرقه در مخلوطی از گازهای H2 و N2 بی تاثیر است زیرا در یک مولکول N2 بین دو اتم نیتروژن پیوند سه گانه برقرار است و به آسانی شکسته نمی شود. مثالی دیگر، آهن در آب بسیار کند واکنش می دهد ولی واکنش پتاسیم در آب بسیار شدید بوده و با تولید شعله همراه است.
 |
نکته:
به طور کلی فلزهای گروه اول از جمله پتاسیم تمایل زیادی دارند تا با از دست دادن یک الکترون به آرایش گازهای نجیب قبل از خود برسند. به همین خاطر فعالیت شیمیایی آن ها بسیار زیاد است.
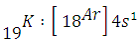
اثر حالت فیزیکی:
برای انجام یک واکنش، واکنش دهنده ها باید در مجاورت یکدیگر قرار بگیرند و با هم مخلوط شوند. بنابراین اگر واکنش دهنده ها در یک فاز باشند، مثلا همگی گاز یا محلول در آب باشند، واکنش با سرعت بیشتری رخ خواهد داد. زیرا در این حالت واکنش دهنده ها بهتر با هم مخلوط شده و در نتیجه احتمال برخورد بین آن ها زیاد می شود و سرعت واکنش هم افزایش می یابد. اما اگر واکنش دهنده ها در دو فاز مختلف باشند مثلا مجاورت یک گاز با یک ماده جامد یا دو مایع مخلوط نشدنی، در این حالت مجاورت واکنش دهنده ها تنها به مرز میان دو فاز بستگی دارد.
یادآوری، تعریف فاز: قسمتی از سامانه که خواص فیزیکی و شیمیایی آن در همه قسمت ها یکسان است.
نکته:
هر ماده جامد به تنهایی یک فاز محسوب می شود. ( فاز را با حالت فیزیکی اشتباه نکنید! )
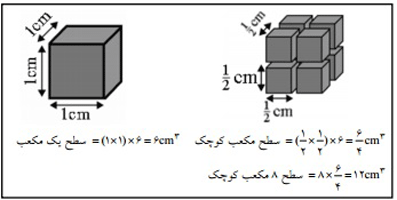
وقتی چند ماده واکنش دهنده به صورت جامد باشند، برای افزایش سرعت واکنش می توان آنها را خرد یا پودر کرد. زیرا در این حالت سطح تماس بین مواد واکنش دهنده بیشتر شده و سرعت نیز بیشتر می شود. از همین مطلب می توان نتیجه گرفت در یک کارخانه تولید کننده نشاسته از آرد گندم، احتمال وقوع انفجار در انبار آرد بیشتر است تا انبار گندم، که این امر بیانگر اثر سطح تماس روی سرعت واکنش است.
راه دیگر برای افزایش سرعت واکنش بین دو ماده جامد استفاده از یک حلال مناسب است. برای مثال در واکنش زیر ضمن ساییدن دو جامد، مقداری از رطوبت موجود در هوا جذب بلورها شده و در مقیاس میکروسکوپی در سطح بلورهای KI و
Pb(NO3)2 فاز محلول (aq) ایجاد می شود و واکنش بین آن ها انجام می گیرد.
پس در نظر داشته باشید، هوای خشک برای انجام این واکنش مناسب نیست.
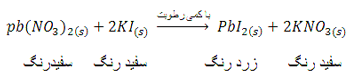
اثر غلظت:
در اغلب واکنش ها، افزایش غلظت واکنش دهنده ها روی سرعت واکنش اثر فزاینده دارد. برای مثال الیاف آهن در هوای معمولی روی شعله، داغ و سرخ می شوند ولی نمی سوزند. ( حدود 21 درصد هوای معمولی را اکسیژن تشکیل می دهد.) اما الیاف آهن که قبلا داغ و سرخ شده اند ( برای تامین انرژی فعال سازی که توضیحات آن در مطالب بعدی ارائه خواهد شد. ) در اکسیژن خالص به شدت می سوزند. تفاوت چشم گیر مشاهده شده در سرعت این واکنش را می توان با افزایش غلظت اکسیژن در واکنش توجیه کرد.
اثر دما:
افزایش دما باعث افزایش برخورد موثر بین واکنش دهنده ها و در نتیجه افزایش سرعت در کلیه واکنش های گرماگیر و گرماده می شود. واکنش فلز منیزیم صیقل داده شده با آب سرد بسیار کند و با آب جوش نسبتا سریع تر است. این اختلاف در سرعت ناشی از اختلاف دما است. دقت داشته باشید در واکنش منیزیم با آب، سرعت واکنش به مرز میان دو فاز وابسته است؛ زیرا منیزیم و آب در دو فاز جداگانه قرار دارند.

















