آنتالپی یک تابع حالت است؟
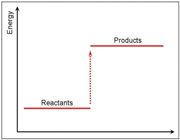
وقتی سطح انرژی فرآورده ها از واکنش دهنده ها بالاتر است، واکنش گرما گیر است.
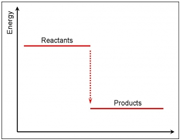
اگر سطح انرزی فرآورده ها پایین تر از مواد اولیه باشد، واکنش گرماده است.
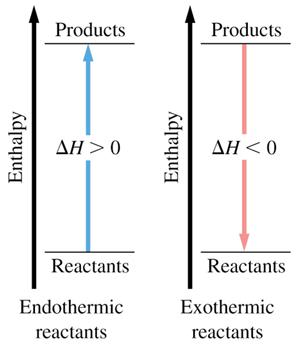
چون اکثر واکنش های شیمیایی در فشار ثابت روی می دهند. تغییر انرژی آن ها همراه با انجام کار توسط سامانه روی محیط یا برعکس است. همواره میزان آنتالپی با انرژی درونی متفاوت است. آنتالپی تغییر انرژی یک سامانه در فشار ثابت است. بنابراین تغییر انرژی واکنش های گرمازا را با آنتالپی منفی و واکنش های گرما گیر را با انتالپی مثبت نمایش می دهیم.
dH = Hfinal – Hinitial
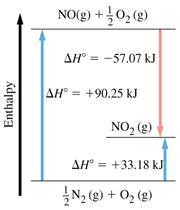
آنتالپی مانند انرژی درونی یک تابع حالت است و اختلاف حالت اولیه آنتالپی با حالت نهایی آن در واکنش شیمیایی، آنتالپی واکنش نامیده می شود و به مسیر واکنش بستگی ندارد. درشکل زیر واکنش از هر روشی صورت گیرد، آنتالپی واکنش 33.18 کیلوژول است.
C8H18(g) +15/2 O2(g) --> 8CO2(g) + 9H2O(g) DH = -5470.5 kJ mol-1
واکنش سوختن اکتان گرما زا است. یعنی 5470.5 کیلوژول بر مول گرما آزاد می شود و علامت منفی است. اما واکنش زیر یک واکنش گرما گیر است و برای انجام شدن نیازمند 11.3 کیلوژول بر مول گرما است.
2HI(g) --> H2(g) + I2(g) DH = + 11.3 kJ mol-1
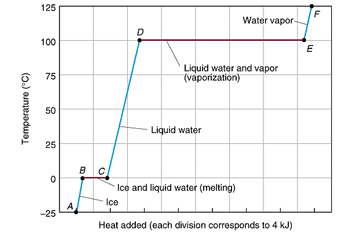
وقتی یخ را گرم کنیم دمای آن بالا می رود تا به صفر درجه برسد. در صفر درجه آب و یخ در حال تعادل هستند. در این حالت افزایش گرما سبب افزایش دما نمی شود. بلکه صرف ذوب شدن یخ می گردد که چون انرژی جذب می شود، تغییر آنتالپی مثبت می باشد.
در دمای صفر درجه چون گرمای اضافه شده صرف ذوب شدن گردیده، افزایش دما نداریم. اما آنتالپی افزایش یافته است. همین وضعیت در نقطه جوش نیز دیده می شود.
بنابراین تبدیل آب مایع به گاز یک فرآیند گرماده است و تبدیل آب جامد به مایع یک فرآیند گرماگیر است.
این وضعیت در تبدیل مایع و گاز و گاز به مایع هم داریم.
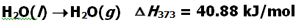
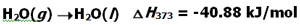
واکنش کلسیم اکسید با آب یک واکنش گرماده است.
واکنش آمونیوم نیترات با آب یک نمونه از فرآیندهای خود به خودی است که در بسته های خنک کننده تجارتی از آن یا آمونیوم کلرید استفاده می شود. در این بسته ها مقدار کمی از این نمک ها به کمک یک غشاء نازک از آب جدا شده اند. وقتی این بسته لمس می شود. غشاء پاره شده و نمک در آب حل می شود. چون این واکنش گرما گیر است. گرما را از محیط جذب کرده و دستان شما خنک می شود.
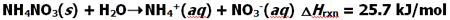
مرکز یادگیری تبیان - تهیه و تنظیم: فاطمه گودرزی