
ترکیب های یون های کمپلکس فلزی
در این بحث، با اشکال و ترکیبات یون های کمپلکسی آشنا می شویم که با استفاده از لیگاندهای تک دندانه (لیگاندهایی که تنها یک پیوند با یون فلزی مرکزی تشکیل می دهند) شکل گرفته اند.
احتمالا با ترکیبات مواد مرکب ساده و نظریه دافعه جفت الکترونی آشنا هستید. متأسفانه این نظریه برای بیش تر یون های کمپلکس فلزی عناصر واسطه صادق نیست. اما در این بحث یاد می گیرید که این ترکیبات آن چنان که به نظر سخت می آیند، نیستند.
- یون های کمپلکس 6 مؤلفه ای:
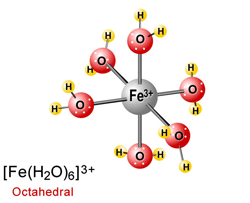
این گروه از یون ها، کمپلکس هایی هستند که یون فلزی مرکزی، 6 پیوند تشکیل می دهد؛ یعنی این یون فلزی مرکزی به سمت 6 لیگاند جذب می شود.

این یون ها شکل هشت وجهی دارند. چهار تا از لیگاندها در یک صفحه قرار دارند و لیگاند پنجم بالای صفحه و لیگاند ششم در پایین این صفحه قرار دارد.

مهم نیست با چه لیگاندی سر و کار دارید، اگر شش تا از آن ها را دارید، شکل های بالا را در هر صورت به خود می گیرند، خیلی راحت!!!
- یون کمپلکس 4 مؤلفه ای:
این یون ها بسیار کم تر مشاهده می شوند و دو شکل متفاوت زیر را می گیرند:
یون های چهار وجهی:
این یون ها بسیار مشابه هم هستند که معمولا در این سطح پدیدار می شوند:
[CuCl4]2- و [CoCl4]2-
یون های مس (II) و کبالت (II) به جای شش تا، چهار یون کلرید دارند که به آن ها وصل شده اند؛ زیرا یون های کلرید آن قدر بزرگ هستند که نمی گذارند یون اضافه ای اطراف یون فلزی مرکزی جا شود.

به خاطر سپردن هر دو مدل، آن قدرها هم سخت نیست!
کمپلکس مسطح مربعی:
گاهی اوقات یک کمپلکس 4 مؤلفه ای به شکل مسطح مربعی از آب در می آید. هیچ راه آسانی برای پیش بینی این که چگونه این کمپلکس تولید می شود، وجود ندارد . یکی از این کمپلکس ها که ممکن است به آن برخورد کنید، سیس پلاتین (cisplatin) است که در شیمی درمانی به عنوان داروی ضد سرطان به کار می رود.
سیس پلاتین (Pt(NH3)2Cl2) یک کمپلکس خنثی است؛ زیرا بار +2 یون پلاتین (Pt) اصلی واقعا با دو بار منفی یون های کلرید خنثی می شود.

پلاتین، دو اتم کلر و دو اتم نیتروژن همگی در یک صفحه قرار دارند.
ایزومری (ترکیب های مشابه) فضایی در یون های کمپلکس:
بعضی از کمپلکس ها می توانند هر دو ایزومری نوری یا هندسی را نشان دهند.
ایزومری هندسی:
این ترکیب های مشابه در کمپلکس های مسطح مانند Pt(NH3)2Cl2 اتفاق می افتد. یون های کلر و آمونیاک به دو روش کاملا متفاوت می توانند خود را اطراف یون مرکزی پلاتین برسانند:

این دو شکل برای Pt(NH3)2Cl2 ایزومر هستند؛ زیرا هیچ راهی نیست که با دوران آن ها حول هر محوری به همدیگر تبدیل شوند . این دو ایزومر همواره در شکل های مشاهده شده باقی می مانند.
کلمات "سیس" و "ترانس" در شیمی آلی هم به کار می روند. ترانس به معنای معکوس است؛ دقت کنید که در این شکل، آمونیاک ها مقابل هم دیگر و کلرها نیز روبروی هم قرار دارند. سیس به معنای در همان سمت است؛ یعنی آمونیاک ها و کلرها نزدیک هم قرار دارند.
ایزومری نوری:
این ایزومرها هیچ صفحه تقارنی ندارند. در شیمی آلی می توانید این مورد را در اتم کربنی که چهار اتم متفاوت به آن متصل شده اند، ببینید.
مثال این مورد می تواند کمپلکس 8 وجهی که شامل یون های لیگاند دو دندانه ای است، باشد:
شکل زیر، ساده شده دو یون بالا را نشان می دهد؛ تمام این یون ها شکل مشابهی دارند و فقط در هدفون های خود فرق دارند!!!

اگر توانسته اید این تصویر را در ذهن خود مجسم کنید، حالا خواهید فهمید که این یون ها هیچ صفحه تقارنی ندارند.


ماده ای که هیچ صفحه تقارنی ندارد، ایزومر نوری دارد؛ یکی از ایزومرها، تصویر آینه ای دیگری است.
یکی از ایزومرها صفحه قطبش نور قطبیده را در جهت عقربه های ساعت دوران می دهد و دیگری آن را خلاف عقربه های ساعت دوران می دهد.

اگر کمی تصورتان را قوی تر کنید؛ خواهید دید که هیچ روشی برای دوران ایزومر دوم در فضا وجود ندارد که عینا مانند اولی به نظر برسد، تنها راه برای قانع کردن خودتان آن است که این دو ایزومر متفاوتند!

















