چند مسئله برای محاسبه استوکیومتری گازها

در درس قبل (روابط حجمی گازها در محاسبات استوکیومتری) با قوانین شارل گی لو ساک و آووگادرو آشنا شدید در این درس با حل چند مسئله به بررسی این قوانین خواهیم پرداخت.
تمرین 1) واکنش موازنه شده ی زیر را در نظر بگیرید. برای جذب 56lit گاز کربن دی اکسید در شرایط استاندارد چند مول لیتیم هیدرو کسید لازم است.
واکنش موازنه شده:
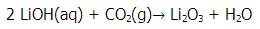
برای توضیح رابطه ی نوشته شده فوق می توان این گونه گفت که طبق معادله ی موازنه شده ی فوق یک مول co2 برای تهیه ی 2 مول LiOH لازم است، از طرفی در شرایط استاندارد هر مول CO2 حجمی معادل 4/22 لیتر حجم دارد، طبق فرض مسئله حجم CO2 موجود 56 لیتر می باشد، پس خواهیم داشت:
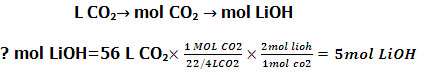
تمرین 2) در شرایطی که چگالی گاز هیدروژن 6/0 گرم بر لیتر است، از واکنش 27/0 گرم آلومینیوم با محلول هیدروکلریک اسید، چند سی سی گاز هیدروژن تولید می شود.
ابتدا می بایستی معادله ی واکنش فوق را نوشت و معادله ی واکنش را موازنه کرد، خواهیم داشت:
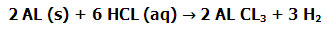
می دانیم که یک مول آلومینیوم 27 گرم است و در این واکنش ما 27/0 گرم آلومینیوم داریم. و از طرفی با توجه به واکنش فوق، در ازای مصرف 2 مول آلومینیوم، 3 مول هیدروژن تولید می شود، با دانستن این موارد می توان نوشت:
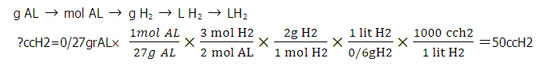
در پایان سعی کنید با حل این مسئله خود را بیازمایید:
تمرین 3) با توجه به واکنش سدیم بی کربنات، حساب کنید که از گرم کردن 5/1 گرم از این ماده چند میلی لیتر گاز کربن دی اکسید تولید می شود، چگالی گاز co2 را در این دما 1/1 گرم بر لیتر در نظر بگیرید.
پاسخ مسئله 14/357 میلی لیتر می باشد؛ آیا پاسخ شما صحیح است؟!

















