فشار اسمزی
در ابتدا با مفاهیم زیر آشنا می شویم :
- غشای نیمه تراوا : غشایی که نسبت به بعضی از اجزای محلول نفوذ پذیر و نسبت به سایرین غیر نفوذ پذیر است. مثل غشاهای سلولی و سلوفان.
- اسمز : حرکت اجزاء از محلولی با غلظت بیشتر به طرف محلولی با غلظت کم تر.
این حرکت برای حلال این گونه توجیه می شود: حرکت حلال از محلولی با غلظت حل شونده ی کم تر به سمت محلولی حاوی غلظت حل شونده ی بیشتر.

- محلول ایزوتونیک : محلولی با فشار اسمزی یکسان در دو طرف یک غشای نیمه تراوا.
- محلول هیپوتونیک : محلولی با فشار اسمزی ای کم تر از محلول هیپرتونیک که دارای فشار اسمزی بالایی است.
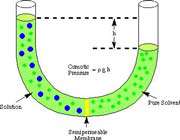
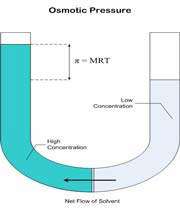
اگر لوله ی U شکل زیر را در نظر بگیرید:
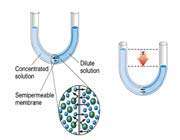
حلال از بازوی سمت راست که دارای محلول رقیق است ( غلظت حلال بیشتر است ) به طرف محلول غلیظ ( محلول شامل آب و نمک ) واقع در بازوی سمت چپ، از طریق غشای نیمه تراوا در حال حرکت است. بنابراین رفته رفته مقدار آب در بازوی سمت چپ افزایش می یابد و محلول رقیق تر می گردد و سطح مایع در لوله بالاتر می رود. در این جا اختلاف فشار به صورت اختلاف ارتفاع در دو سمت بازو ایجاد می شود که به صورت فشار در شکل ظاهر شده است. این فشار را فشار اسمزی می نامند.
فشار اسمزی به صورت زیر توسط جاکوب وانت هوف ( Jacobus Henricus van"t Hoff ) فرمول بندی شده است:

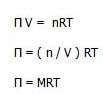
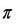 نشان دهنده ی فشار اسمزی، R ثابت گاز ایده آل، M مولاریته ی محلول بر حسب مول در لیتر و T دما را بر حسب کلوین نشان می دهد.
نشان دهنده ی فشار اسمزی، R ثابت گاز ایده آل، M مولاریته ی محلول بر حسب مول در لیتر و T دما را بر حسب کلوین نشان می دهد.
ماهیت فشار اسمزی
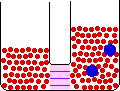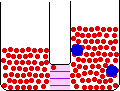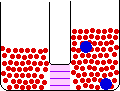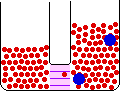
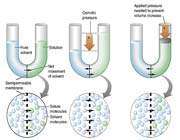
غشایی مانند سلوفان که برخی از مولکول ها ، نه همه آنها ، را از خود عبور میدهد، غشای نیمه تراوا نامیده میشود. غشایی را در نظر میگیریم که بین آب خالص و محلول قند قرار گرفته است. این غشا نسبت به آب ، تراوا است، ولی «ساکارز» (قند نیشکر) را از خود عبور نمیدهد. در شروع آزمایش ارتفاع آب در بازوی چپ لوله U شکل برابر با ارتفاع محلول قند در بازوی راست این لوله است. از این غشا ، محلول های قند نمیتوانند عبور کنند، ولی مولکول های آب در هر دو جهت میتوانند عبور کنند.
در بازوی چپ لوله فوق (بازویی که محتوی آب خالص است)، تعداد مولکول های آب در واحد حجم بیش از تعداد آنها در بازوی راست است. از اینرو ، سرعت عبور مولکول های آب از سمت چپ غشا به سمت راست آن بیشتر از سرعت عبور آنها در جهت مخالف است. در نتیجه ، تعداد مولکول های آب در سمت راست غشا به تدریج زیاد میشود و محلول قند رقیقتر میگردد و ارتفاع محلول در بازوی راست لوله U زیاد میشود. این فرایند را اسمز مینامند.
اختلاف ارتفاع در سطح مایع در دو بازوی لوله U ، اندازه فشار اسمزی را نشان میدهد. بر اثر افزایش فشار هیدروستاتیکی در بازوی راست که از افزایش مقدار محلول در این بازو ناشی میشود، مولکول های آب از سمت راست غشا به سمت جپ آن رانده میشوند تا اینکه سرانجام سرعت عبور از سمت راست با سرعت عبور از سمت چپ برابر گردد.
بنابراین حالت نهایی یک حالت تعادلی است که در آن ، سرعت عبور مولکولهای آب از غشا در دو جهت برابر است.
پدیده ی اسمز در گلبول های قرمز بدن نیز وجود دارد. به این صورت که اگر گلبول های قرمز خون را در محلول آب خالص قرار دهیم، مولکول های آب از جداره ی نیمه تراوای گلبول قرمز عبور کرده و به درون گلبول قرمز راه می یابند. غلظت حلال آب که در اطراف سلول خونی بیشتر بوده و حال به درون سلول خونی راه یافته اند، در نتیجه مقدار آب درون گلبول رفته رفته افزایش یافته و منجر به پاره شدن جداره ی سلول خونی می شود.
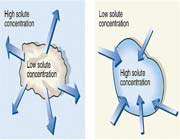
اما اگر همین گلبول در محیط آب و نمک قرار گیرد، چون دارای حلال بیشتری است آب از گلبول به محیط اطراف نفوذ می کند و در نتیجه منجر به چروکیده شدن گلبول می شود. بنابراین در تزریقات وریدی بایستی از محلول هایی ( ایزوتونیک )استفاده شود که دارای فشار اسمزی یکسان با فشار اسمزی خون باشند.
زمانی که در لوله ی U شکل، آب از غشای نیمه تراوا عبور می کند و فشار اسمزی را ایجاد می سازد، به علت فشار هیدروستاتیکی محلولی که دارای غلظت حلال بیشتری است، آب مجددا از همان بازو به بازوی دیگری در لوله ی U شکل جریان می یابد تا زمانی که سرعت عبور آب در دو طرف غشا برابر شود در نتیجه فشار تعادلی نیز برقرار می گردد.
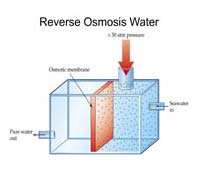
حال اگر فشاری بیشتر از فشار تعادلی بر روی بازوی شامل حلال و ماده ی حل شده وارد گردد، حلال آب مجددا از همان بازو به بازوی دیگری جریان می یابد و پدیده ی اسمز معکوس صورت می گیرد.
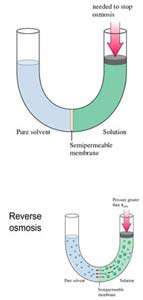
از روش اسمز معکوس برای خالص سازی آب دریا نیز استفاه می شود.
مرکز یادگیری سایت تبیان گردآورنده و تنظیم: نوربخش

















